La pandemia por COVID-19 que golpeó al mundo en 2020 ha desencadenado varias emergencias que se propagaron en paralelo con la epidemia viral. Entre ellas, se produjo una diseminación masiva de información o «infodemia» sobre la enfermedad y sus tratamientos, que se canalizó a través de la prensa, la web y las redes sociales. Este exceso de información resulta cada día más difícil de combatir por las Autoridades Sanitarias. Abarca desde debate sobre el origen del SARS-CoV-2 (natural o artificial), su liberación (accidental o intencional), hasta las oportunidades para las compañías farmacéuticas que desarrollan sus vacunas. Fue favorecida por la hiperconexión actual de personas, dada por el uso generalizado de teléfonos inteligentes, fácil acceso a internet, redes sociales y servicios de mensajería multiplataforma. Esta infodemia incluyó información sobre medicamentos distorsionada, sensacional, y muchas veces con débil evidencia científica que influyeron tanto a los líderes de opinión como a personas activas en las redes sociales, lo cual afectó las elecciones de pacientes en todo el mundo.
Se ha difundido información sobre algunos medicamentos aprobados para otras indicaciones como la Cloroquina, Hidroxicloroquina, medicamentos antiinflamatorios no esteroideos (AINEs), inhibidores de la enzima convertidora de angiotensina (IECA), antagonistas de los receptores de angiotensina II (ARAS II), medicamentos para el tratamiento del ébola, antivirales y otros medicamentos, que podrían haber llevado a un uso inapropiado de los mismos.
Cloroquina e Hidroxicloroquina
En 2003, la Cloroquina se utilizó por primera vez para el tratamiento de coronavirus SARS-CoV en combinación con medicamentos antivirales (Lopinavir y Ritonavir). Dada la alta similitud genética entre SARS-CoV-2 y SARS-CoV, Cloroquina e Hidroxicloroquina fueron inmediatamente atractivos para
investigación en el tratamiento de COVID-19. Los medios de comunicación forzaron el mensaje de que estos medicamentos eran efectivos tanto para tratar como para prevenir la infección por SARS-CoV-2. Esta tormenta de información tuvo un impacto perjudicial en la cadena de suministro, disponibilidad y patrones de uso. Varios países se apresuraron a almacenar estos medicamentos, llegando a frenar exportaciones. Mientras tanto, el público comenzó a comprarlos frenéticamente sin receta médica, para garantizar la disponibilidad de un stock de emergencia, reduciendo así el suministro para pacientes que reciben estos medicamentos para enfermedades reumáticas. Pacientes saludables comenzaron a tomar dosis no controladas de estos medicamentos, creyendo que podrían prevenir COVID-19, resultando en casos de intoxicación. Varias reacciones adversas graves fueron reportadas, como muerte súbita cardíaca debido a arritmia y prolongación del intervalo QT.
Mehra et al. publicaron los resultados del primer estudio observacional multinacional para analizar datos de 96.032 pacientes, mostrando que la Hidroxicloroquina no era efectiva en el tratamiento de COVID-19, disminuía la supervivencia hospitalaria y aumentaba arritmias ventriculares. Este estudio fue ampliamente cuestionado en la comunidad científica debido a limitaciones metodológicas, conduciendo finalmente a la retracción del artículo.
Para abordar esta crisis, las Autoridades Sanitarias adoptaron estrategias de comunicación, emitiendo alertas de seguridad y notas aclaratorias. La Organización de la Salud (OMS) suspendió los ensayos clínicos sobre medicamentos antipalúdicos debido a los problemas de seguridad emergentes reportados por Mehra et al. Después de que el artículo fue retirado, la OMS reanudó las investigaciones sobre el uso de estos medicamentos.
IECA y ARAS II
Medicamentos que actúan sobre el sistema renina-angiotensina-aldosterona (SRAA), como los IECA y ARAS-II, probablemente desencadenaron el mayor debate. Esto se debió al papel fundamental de la proteína ACE-2, tanto en la entrada del virus SARS-CoV-2 como en la modulación de citocinas responsables de inflamación en los pacientes. Dado que las proteínas de pico del coronavirus interactúan con la proteína ACE-2 para ingresar a las células humanas y que los IECA y los ARAS-II pueden inducir la regulación positiva de la enzima ACE2, se postuló que los medicamentos antihipertensivos pueden favorecer la entrada de virus en la célula huésped. Sin embargo, ACE-2 (a través de la vía de Mas ACE2/Ang (1-7)) es un modulador negativo del SRAA, que a su vez inhibe la liberación de varias citoquinas inflamatorias. Por lo tanto, estos medicamentos podrían ejercer efectos tanto beneficiosos como perjudiciales en diferentes etapas de la enfermedad.
La discusión sobre el papel central de ACE-2 en COVID-19 y el posible efecto modulador de los medicamentos que se dirigen a esta enzima comenzó con una carta de Fang et al. a The Lancet. Esta carta revisa tres conjuntos de casos notificados en China, y destacaron un importante porcentaje de pacientes con hipertensión y diabetes (12-30%). El difícil debate sobre los resultados de la modulación ACE-2 permaneció confinado a la comunidad científica hasta que la carta comenzó a circular en línea.
Los IECA y los ARAS-II tienen un papel fundamental en la profilaxis y tratamiento de varias enfermedades cardiovasculares, y muchos pacientes en todo el mundo estaban recibiendo tratamiento con ellos. La difusión incontrolada de noticias sobre su presunto papel en favorecer la infección por SARS-CoV-2 podría haber afectado el cumplimiento del tratamiento en muchos pacientes con serias implicaciones para su salud.
Algunas Autoridades Sanitarias e instituciones científicas refutaron esta noticia y recomendaron que las terapias con medicamentos antihipertensivos no se modificarán hasta que se cuente con mayor evidencia derivada de los estudios en curso. Los primeros resultados de algunos de estos estudios mostraron que estos medicamentos no tienen influencia en la prognosis de los pacientes con COVID-19.
Antiinflamatorios no esteroideos (AINEs)
Se encuentra descrito que los AINEs pueden reducir la inflamación y fiebre de una infección, enmascarando y retrasando la detección de síntomas de la misma. Fang et al. señalaron que los AINEs, particularmente Ibuprofeno, podrían aumentar la expresión ACE-2, favoreciendo la infección por SARS-CoV-2. Sin embargo, la única evidencia que respalda la regulación positiva de ACE-2 asociada con Ibuprofeno es un estudio sobre un modelo de fibrosis cardíaca en ratas.
El 14 de marzo de 2020, el Ministro de Salud francés tuiteó una advertencia contra el uso de AINE porque potencialmente infección agravada por COVID-19. Esto desencadenó una explosión de alertas publicadas en redes sociales, que luego fueron amplificados por artículos en periódicos. Tal comunicación generalizada tuvo un gran impacto en pacientes y profesionales de la salud, llevando a una disminución en el uso general y la prescripción de Ibuprofeno y otros AINEs.
Varias Autoridades Sanitarias comentaron las declaraciones por las autoridades francesas. La OMS informó que no hay estudios sobre medicamentos antiinflamatorios vinculados con mayor tasa de mortalidad por COVID-19. La Agencia Europea de Medicamentos (EMA) informó que no había evidencia para establecer si el Ibuprofeno pudiese agravar el estado de los pacientes con COVID-19. Recomienda que los pacientes que lo toman no deben suspender el tratamiento, particularmente aquellos en tratamiento crónico. La FDA comunicó sobre la falta de evidencia para apoyar las advertencias sobre el Ibuprofeno.
Infodemia y farmacovigilancia
Los medicamentos utilizados en el tratamiento de COVID-19 se han convertido en un motivo de preocupación para la farmacovigilancia. Se han generado dos situaciones que se encuentran esquematizadas en la Figura 1. En la primera situación, los medicamentos ya aprobados para otras indicaciones han sido catalogados como peligrosos debido a su capacidad para promover la infección en sujetos sanos o provocar complicaciones en pacientes con enfermedad. La principal consecuencia podría ser que los pacientes que estaban tomando estos medicamentos para las indicaciones aprobadas podrían suspender voluntariamente la terapia, con el riesgo de un empeoramiento grave de sus enfermedades subyacentes. Este fue el caso de los IECA, ARAS-II y AINEs.
En la segunda situación, algunos medicamentos que ya están comercialmente disponibles para otras indicaciones se han promovido como particularmente efectivos a pesar de la falta o ausencia de evidencia científica. Esto provocó un apuro por adquirir el medicamento, lo que luego significó que a los pacientes que utilizan estos medicamentos para indicaciones aprobadas no contaran con sus tratamientos. Este fue el caso de la Cloroquina e Hidroxicloroquina. Un segundo efecto fue la toma de medicamentos sin supervisión médica. Esta situación puede tener como consecuencia la sobredosis, toma sin justificación terapéutica y autoadministración de preparaciones peligrosas con nombres o contenidos similares a los de los medicamentos aprobados, con el consiguiente riesgo de intoxicación. En este escenario, los involucrados en farmacovigilancia enfrentan diferentes desafíos (ver Figura 2). En primer lugar, los gobiernos, Autoridades Sanitarias y fabricantes deben colaborar para estimular y apoyar a la academia e instituciones de investigación en la realización de estudios para asegurar que el perfil riesgo-beneficio de los candidatos de medicamentos para el tratamiento de COVID-19 es adecuado. Esto incluye no solo estudios clínicos, sino también observacionales, particularmente los de evidencia del mundo real. Otro desafío es la implementación de sistemas de reporte espontáneo. En situaciones donde el perfil riesgo-beneficio no está claro, es importante evaluar la seguridad del medicamento estimulando la notificación espontánea de eventos adversos, particularmente informes provenientes de pacientes, dada la probabilidad de problemas relacionados con la automedicación. La detección de señales también merece atención. Podemos esperar que la pandemia tenga efectos importantes en las tendencias de informes espontáneos, para medicamentos involucrados tanto en el tratamiento de COVID-19 como para otras patologías. Por lo tanto, las Autoridades Sanitarias, la academia y los titulares de autorización de comercialización tendrá que considerar el «factor pandémico» en la interpretación de la información obtenida para la detección de señales.
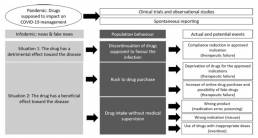
Figura 1: Efectos «infodémicos» en las actitudes de las personas en torno a la toma de medicamentos y sus posibles consecuencias.
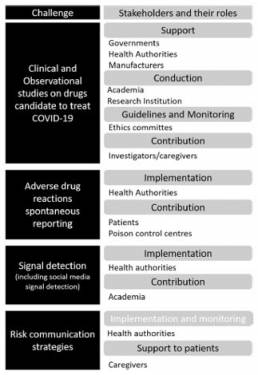
Figura 2: Desafíos para las actividades de farmacovigilancia
La pandemia ha ejercido presión sobre los sistemas de salud, incluidos los sistemas de farmacovigilancia, en todo el mundo. Los sistemas disponibles probablemente no estaban listos para manejar una emergencia de proporciones tan grandes y con características tan impredecibles.
El papel de la farmacovigilancia en el manejo de tales emergencias es crucial, específicamente en el uso apropiado de los medicamentos propuestos para tratar la enfermedad y el manejo de consecuencias reales o potenciales del uso inapropiado de los mismos. Estos desavíos y otros probablemente surjan una vez que las vacunas estén disponibles.
Referencia:
Noticia_Infodemic Farmacovigilancia

La sostenibilidad como parte de cómo construimos futuro
Presentamos nuestro primer Informe de Sostenibilidad, un reflejo de cómo integramos la responsabilidad ambiental, social y de gobernanza en la…
Día de la obstetricia y la embarazada
¿Cómo se transforma la incertidumbre en una experiencia segura y asombrosa? Con una conexión única que hace de cada embarazo un viaje inolvidable.…
Los alimentos ricos en potasio mejoran la salud cardiovascular de las mujeres
De acuerdo con la Organización Mundial de la Salud (OMS), las enfermedades cardiovasculares (ECV) son la principal causa de muerte en todo el mundo y…
Viruela del mono: la OMS declara alerta máxima por el aumento de casos en el mundo
La Organización Mundial de la Salud ha declarado este sábado 23 de julio a la viruela de mono como una emergencia sanitaria internacional luego de un…




