Pirfenidona es un medicamento de administración oral indicado para la fibrosis pulmonar idiopática. El producto en su presentación de cápsulas fue aprobado en Estados Unidos por la FDA en el año 2014. (1,2,3) Estudios in vitro han mostrado que produce efectos antifibróticos, antiinflamatorios y antioxidantes.
Informes iniciales de China luego corroborados con datos del norte de Italia, sugirieron que el grupo demográfico más gravemente afectado por COVID-19 eran los hombres de edad avanzada. Los factores de mal pronóstico incluían antecedentes de tabaquismo y presencia de comorbilidades como hipertensión, diabetes mellitus y enfermedad coronaria. Esto también fue observado en el estudio chino de Guan y colaboradores, realizado en 1099 pacientes con COVID-19. (6) El grupo en el que la infección por SARS-CoV-2 es más letal es muy representativa de los pacientes que padecen fibrosis pulmonar idiopática (FPI), patología que afecta característicamente a los hombres en su séptima u octava década de vida, comúnmente con comorbilidades como hipertensión, diabetes y cardiopatía isquémica, y con antecedentes de exposición al humo de cigarrillo. (4)
La FPI es una enfermedad progresiva en la que la función pulmonar disminuye inexorablemente, lo que lleva a insuficiencia respiratoria y finalmente a la muerte, siendo el trasplante de pulmón el único tratamiento que mejora los resultados. Una gran proporción de pacientes con FPI son tratados con uno de los dos fármacos antifibróticos disponibles, Pirfenidona y Nintedanib, que han demostrado que disminuyen la tasa de disminución de la función pulmonar.
La justificación del uso de la terapia antifibrótica en pacientes con COVID-19, se basa en el espectro de la enfermedad fibrótica pulmonar observada en COVID-19, que va desde la fibrosis asociada con la presencia de neumonía, hasta lesión pulmonar aguda grave en la que hay evolución a un cambio fibrótico generalizado. La fibrosis pulmonar generalmente está presente en la autopsia de los pacientes fallecidos. En un estudio en el que estudiaron 159 autopsias de pacientes con síndrome respiratorio agudo (SRA), se observó fibrosis en el 4% de los pacientes con duración de la enfermedad menor a 1 semana, 13% de los pacientes con duración de la enfermedad entre 1 y 3 semanas, y 61% de los pacientes con duración de la enfermedad mayor a tres semanas. Esto sugiere que las terapias antifibróticas deben ser consideradas luego de la primera semana del inicio de la SRA para ser efectivas. (4)
En algunos casos, los mecanismos inmunes anormales inician y promueven la fibrosis pulmonar, posiblemente como consecuencia de una tormenta de citocinas. Sin embargo, el daño alveolar difuso, que es la característica definitoria del SRA, ha sido la característica histológica observada en el COVID-19 mortal, con la presencia adicional de trombosis microvascular. (4)
Pirfenidona es un medicamento antifibrótico que muestra una efectividad en la atenuación de la tasa de disminución de la función pulmonar en aproximadamente un 50% . Esta terapia es ampliamente considerada por mejorar la esperanza de vida en 2 a 5 años. Teniendo en cuenta que las estimaciones históricas de supervivencia media para esta afección son de 3 años desde el diagnóstico, cualquier decisión de suspender el tratamiento debe considerarse cuidadosamente. (4)
Es una piridona con un mecanismo de acción poco conocido. Aunque tiene efectos pleiotrópicos, no es inmunosupresor per se, por lo que no existe una justificación para su suspensión ante una infección viral o bacteriana. (4)
Estudios in vitro en fibroblastos de pulmón humano han mostrado que la Pirfenidona anula la síntesis de colágeno estimulado por TGF-β1, mediante la inhibición de la regulación positiva de HSP47 y Col1 ARN, de manera concentración-dependiente. Estudios experimentales en células hepáticas estrelladas de rata muestran que la Pirfenidona bloquea los efectos proliferativos de PDGF de manera concentración-dependiente. En un estudio con fibroblastos pulmonares humanos, esta sustancia mostró reducción en la proliferación de fibroblastos mediante la producción de actina de células alfa del músculo liso inducida por TGF-β, así como la reducción de los niveles de procolágeno. (3)
En un modelo in vivo de lesión de pulmón aguda inducida por lipopolisacárido murina y shock endotóxico, la Pirfenidona reguló negativamente las citoquinas proinflamatorias como TNF-α, IFN-γ, and interleuquina (IL)-6, y mejoró la supervivencia. En modelos in vitro tanto humanos (en linfocitos sanguíneos periféricos) y modelos in vivo de ratón, este activo ejerce un efecto antiinflamatorio similar, inhibiendo la proliferación de la enterotoxina B estafilococcal y la síntesis de TNF-α, IFN-γ, IL-1β, and IL-6. (3)
Con respecto a sus propiedades antioxidantes, ha sido observado que Pirfenidona puede actuar como un captador de los radicales libres hidroxilo y superóxidos. En microsomas hepáticas de oveja, esta sustancia bloquea la peroxidación lipídica dependiente de NADPH en forma concentración-dependiente. (3)
Los efectos de Pirfenidona en modelos animales de fibrosis pulmonar inducida por bleomicina sugieren una atenuación en el desarrollo de la enfermedad. En hámster, la Pirfenidona fue administrada dos días antes de una dosis simple de bleomicina, o luego de la segunda de tres semanas de administración de esta sustancia. Se visualizó una atenuación significativa en el desarrollo de la fibrosis, así como una reducción en los marcadores de estrés oxidativo e inflamación neutrofílica. (3)
Es posible que las terapias antifibróticas desarrolladas para las enfermedades pulmonares fibróticas crónicas puedan ser beneficiosas en COVID-19, tanto en la fase aguda de la enfermedad como en la prevención de complicaciones a largo plazo. Las posibles terapias antifibróticas podrían tener efectos beneficiosos en el tratamiento de esta enfermedad a través de una variedad de mecanismos diferentes (ver Figura 1), como prevenir la absorción y replicación viral, inhibir la señalización viral y a través de efectos beneficiosos en el sistema renina-angiotensina. (4)
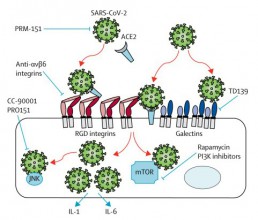
Figura 1: Mecanismos potenciales a través de los cuales los nuevos fármacos antifibróticos podrían prevenir el desarrollo de infección grave por SARS-CoV-2. (4)
La formulación inhalada de Pirfenidona se está evaluando en pacientes con COVID-19. (5)
Dada la rápida propagación global del COVID-19 y con los esfuerzos centrados en gran medida en el tratamiento de los pacientes con neumonía por COVID-19 más gravemente enfermos, las comunidades clínicas y de investigación de FPI han tenido poco tiempo para recopilar datos suficientes para evaluar a fondo los riesgos y beneficios potenciales de iniciar y continuar la terapia antifibrótica en los pacientes afectados. Todavía no hay datos que reporten la incidencia o mortalidad de la infección por SARS-CoV-2 en pacientes con FPI. Sin embargo, estos pacientes se debilitan aún más por la reducción de la reserva pulmonar, por lo que es posible que el pronóstico sea aún peor para los pacientes con FPI que para la población general. Los estudios futuros que analicen el efecto de la pandemia de COVID-19 sobre la incidencia de exacerbación aguda de la FPI serán informativos para establecer el vínculo postulado con la infección viral. (4)
Dosis y administración (2)
Debe administrarse con comidas.
La dosis recomendada es de 801 mg tres veces por día (2403 mg/día).
Luego del inicio del tratamiento, se debe valorar la dosis completa de 2403 mg/día en un período de 14 días de tratamiento, como sigue:
Se debe considerar la reducción temporal de dosis, interrupción o descontinuación en caso de reacciones adversas. Previo al tratamiento se debe realizar un test hepático.
Precauciones y advertencias
Elevación de las enzimas hepáticas (ALT, AST y bilirrubina) y daño hepático (incluida lesión hepática grave con resultado de muerte) han sido reportados. Se deben monitorear los niveles ALT, AST y bilirrubina antes y durante el tratamiento. (2)
Se ha observado fotosensibilidad y erupción. Se debe evitar la exposición a la luz solar y las lámparas solares, usar protector solar y ropa protectora diaria. (2)
Se han producido náuseas, vómitos, diarrea, dispepsia, enfermedad por reflujo gastroesofágico y dolor abdominal. Se pueden reducir o suspender temporalmente las dosis según sea necesario. (2)
Se debe evitar la Pirfenidona si los pacientes tienen una tasa de filtración glomerular estimada de menos de 30 mL/min por 1,73 m2. Aunque solo 1,6% de los pacientes en la cohorte informada por Guan et al tenían una concentración de creatinina de 133 μmol/L o más, esta proporción aumentó a 4,3% con COVID grave. Estos datos implican que los pacientes con SARS-CoV leve tienen menos probabilidad de padecer disfunción renal, pero con el aumento de la gravedad de la enfermedad COVID-19, esta disfunción renal podría convertirse en una consideración importante al considerar las terapias antifibróticas. (6)
Eventos adversos
Las reacciones adversas más comunes (≥10%) son nauseas, erupción cutánea, dolor abdominal, infección del tracto respiratorio superior, diarrea, fatiga, dolor de cabeza, dispepsia, mareos, vómitos, anorexia, enfermedad por reflujo gastroesofágico, sinusitis, insomnio, disminución de peso y artralgia. (2)
Puede asociarse con hepatotoxicidad. La disfunción hepática es común en pacientes infectados con SARS-CoV-2. Se observaron concentraciones elevadas de enzimas hepáticas en 22% pacientes con COVID-19 confirmado y 39% con enfermedad grave. El uso concomitante de antibióticos para la infección bacteriana superpuesta es probable que aumente el riesgo de disfunción hepática, por lo que, en el contexto de un paciente hospitalizado que tiene FPI y COVID-19 grave con pruebas de función hepática alteradas, puede ser necesario suspender temporalmente la terapia antifibrótica en espera de la resolución de la disfunción hepática. (6)
Referencias
(1) Food and Drug Administration (FDA). FDA Approved Drugs. Disponible en:
https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=022535
(2) Inserto ESBRIET. Food and Drug Administration. 2019. Disponible en:
https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/022535s012,208780s002lbl.pdf
(3) Margaritopoulos GA, Vasarmidi E, Antoniou KM. Pirfenidone in the treatment of idiopathic pulmonary fibrosis: an evidence-based review of its place in therapy. Core Evid. 2016;11:11-22. Published 2016 Jul 1. doi:10.2147/CE.S76549. Disponible en:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4936814/
(4) Peter M George, MD; Prof Athol U Wells, MD; Prof R Gisli Jenkins, PhD. Pulmonary fibro-sis and COVID-19: the potential role for antifibrotic therapy. 15 de mayo 2020. doi: https://doi.org/10.1016/S2213-2600(20)30225-3. Disponible en:
https://www.thelancet.com/journals/lanres/article/PIIS2213-2600(20)30225-3/fulltext
(5) Clinical Trials. A Study to Evaluate the Efficacy and Safety of Pirfenidone With Novel Coronavirus Infection. NCT04282902. Disponible en:
https://www.clinicaltrials.gov/ct2/show/NCT04282902
(6) Guan WJ Ni ZY Hu Y et al. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020; 382: 1708-1720. DOI: 10.1056/NEJMoa2002032. Disponible en:
https://www.nejm.org/doi/full/10.1056/NEJMoa2002032
Conexion Pirfenidona
La sostenibilidad como parte de cómo construimos futuro
Presentamos nuestro primer Informe de Sostenibilidad, un reflejo de cómo integramos la responsabilidad ambiental, social y de gobernanza en la…
Día de la obstetricia y la embarazada
¿Cómo se transforma la incertidumbre en una experiencia segura y asombrosa? Con una conexión única que hace de cada embarazo un viaje inolvidable.…
Los alimentos ricos en potasio mejoran la salud cardiovascular de las mujeres
De acuerdo con la Organización Mundial de la Salud (OMS), las enfermedades cardiovasculares (ECV) son la principal causa de muerte en todo el mundo y…
Viruela del mono: la OMS declara alerta máxima por el aumento de casos en el mundo
La Organización Mundial de la Salud ha declarado este sábado 23 de julio a la viruela de mono como una emergencia sanitaria internacional luego de un…




