IVERMECTINA: Un nuevo soldado contra la lucha de COVID-19.
Un estudio in vitro conducido por el Instituto Monash de Descubrimientos en Biomedicina (BID) y el Hospital Real de Melbourne de Australia, ha mostrado que Ivermectina es capaz de detener la replicación viral de SARS-CoV-2 en menos de 48 hs.
Previamente, mediante estudios in vitro, Ivermectina mostró ser efectivo contra diversos virus como VIH, Zika, Dengue e Influenza. Teniendo presente dichos hallazgos, Caly y colaboradores han decidido estudiar el comportamiento de este medicamento en células Vero-hSLAM infectadas previamente con SARS-CoV-2. Mediante PCR, luego de 24 horas de incubación con el medicamento se observó una reducción del 93% en la carga viral de ARN. A las 48hs de incubación con el medicamento se observó la pérdida efectiva de la carga viral esencial (disminuyendo más de 5.000 veces respecto a condiciones iniciales, 99.8%) en las células infectadas y en su sobrenadante. De esta forma Ivermectina mostró in vitro su acción antiviral para SARS-CoV-2 en una sola dosis, en un período de 24-48 hs.
¿Qué es Ivermectina y cómo inhibe SARS-CoV-2?
Se trata de un antiparasitario descubierto en la década de los años 70, que resultó revolucionario por su amplio espectro, al actuar contra nemátodos y artrópodos. Si bien inicialmente fue utilizado en animales, desde 1988 ha sido usado exitosamente en humanos, mejorando la nutrición y calidad de vida de billones de personas. Ha mostrado ser seguro, eficaz y bien tolerado para diversas infecciones parasitarias (en especial Oncocercosis).
Ivermectina es un inhibidor de la interacción entre las proteínas de la envoltura viral y la célula huésped. Los autores plantean que, de la misma forma que ocurre con VIH, Zika, Dengue e Influenza; Ivermetcin inhibe la importación viral al núcleo. Esto lo logra ya que interacciona con la proteína citosólica de importación nuclear IMPα/β1, e impide su unión con las proteínas de la cápside viral.
El uso de Ivermectina en la actualidad
Recientemente se obtuvieron los resultados preliminares de un estudio clínico con Ivermectina, donde 704 pacientes con Covid-19 fueron tratados con Ivermectina, a una dosis de 150ug/Kg. Por otra parte, otros 704 pacientes fueron incluidos para ser tratados con placebo. Se observó que la tasa de letalidad y la permanencia en el hospital fue menor para los pacientes tratados con Ivermectina, pero el autor declara que aún es necesario confirmar estos hallazgos mediante más estudios clínicos randomizados.
En República Dominicana, el Dr. Tavárez ha reportado que ha tratado varios pacientes con Ivermectina, y ha obtenido respuesta favorable en todos los casos, sin registrar casos fatales. De manera similar, en Perú también han tratado pacientes con Covid-19 con Ivermectina, con una mejoría del 100% y resolución de la fiebre dentro de las 48 horas de iniciado el tratamiento. En Perú, el Dr. Aguirre publicó el 02 de Mayo un artículo titulado “INCLUSIÓN DE LA IVERMECTINA EN LA PRIMERA LÍNEA DE ACCIÓN TERAPÉUTICA PARA COVID-19”, donde presenta un plan terapéutico para Covid-19 con Ivermectina, teniendo en consideración lo anteriormente mencionado. El autor expresa como conclusión que “Al no existir prácticamente riesgo en el uso de la Ivermectina, se recomienda formalizar su inclusión en la primera línea de acción terapéutica para COVID-19, para reducir la carga y replicación viral”.
Actualmente Ivermectina no está presente dentro de los medicamentos más evaluados en estudios clínicos, a pesar de sus resultados in vitro prometedores y su uso fuera de las indicaciones presuntamente exitosos. Los fármacos más estudiados son: Lopinavir/Ritonavir, Remdesivir, Cloroquina, Interferón, Hidroxicloroquina y Azitromicina.
Ivermectina está aprobado por FDA para su uso como antiparasitario en humanos y animales, pero aún no ha sido aprobado para su uso en Covid-19. Esta aprobación dependerá de los resultados de más pruebas preclínicas y clínicas que confirmen los resultados recientemente obtenidos. Este medicamento ya está disponible en todo el mundo; con lo cual, de ser aprobado para su tratamiento en COVID-19, su aplicación para COVID-19 podría ser inmediata.
Bibliografía:
– Periódico El Caribe. Medicamento ayuda a 150 con COVID19 en centro de Puerto Plata (20 Abril 2020). Disponible en:
https://www.elcaribe.com.do/2020/04/20/medicamentoayuda-a-150-con-covid-19-en-centro-de-puerto-plata/
– Aguirre G. inclusión de la Ivermectina en la primera línea de acción terapéutica para Covid-19. Mayo 2020. Perú.
– Ivermectin. FDA. 2020. Extraído de:
https://www.fda.gov/animal-veterinary/product-safety-information/faq-covid-19-and-ivermectin-intended-animals
IVERMECTINA Un nuevo soldado en la lucha contra COVID-19.

Vacunas en desarrollo para tratamiento de infecciones con SARS-CoV-2
Los primeros casos de infecciones por un virus respiratorio ocurrieron en China, en el último trimestre de 2019. La elevada capacidad replicativa e infectiva de este virus lo convirtió en epidemia y prontamente en pandemia. Fue el 11 de Enero de 2020 que se logró obtener la secuencia de este virus y caracterizarlo como SARS-CoV-2. Desde ese momento se desencadenó el desarrollo masivo de candidatos a vacunas para este virus, y fue el 16 de Marzo de 2020 cuando comenzó el primer estudio clínico para analizar la eficacia de una vacuna candidata basada en ARN.
La OMS mantiene actualizado el panorama de los candidatos de vacunas de Covid-19. Actualmente hay 5 vacunas candidatas siendo evaluadas en ensayos clínicos, y 71 vacunas candidatas en evaluación pre-clínica.. Si bien hay más vacunas candidatas, las mismas no se encuentren en estados de desarrollo e investigación previa a la etapa pre-clínica in vivo; o no han confirmado su etapa de desarrollo a las autoridades. Estados Unidos es responsable del 46% de la actividad del desarrollo de estas vacunas, China del 18%, el resto de Asia+ Australia del 18%, y Europa es responsable del 18% restante.
La diversidad del desarrollo en los tipos de vacunas se ha desplegado para poder utilizar la tecnología disponible para ganar la batalla contra el SARS-CoV-2. Los tipos de vacunas varían entre: virus vivos atenuados, inactivados, vectores virales no replicantes, vectores virales replicantes, proteínas recombinantes, basadas en péptidos, ADN y ARN. Algunos de estos tipos de vacunas no han sido aprobadas previamente como vacunas, pero se han utilizado en oncología y esto ha alentado a los científicos a explorar su aplicación en la vacuna para SARS-CoV-2. Las vacunas basadas en ADN y ARN ofrecen flexibilidad para manipular el antígeno y por tanto permiten realizar cambios en las mismas más prontamente. El antígeno que los desarrolladores de vacunas buscan neutralizar suele ser, para la mayoría de las candidatas, la proteína viral espiga (spike protein).
El desafío de desarrollar una vacuna para tratar esta pandemia no tiene precedentes, lo cual ha generado investigaciones clínicas y pre-clínicas a velocidades inimaginadas. Se cree que una vacuna para esta indicación podría estar disponible para comienzos del 2021; lo cual es extremadamente rápido dado el tiempo que se requiere usualmente (5-10 años aproximadamente). Estas vacunas candidatas deben ser evaluadas cuidadosamente para certificar la eficacia y seguridad en cada paso.
Bibliografía:
– Le et al. The Covid-19 vaccine development landscape. Nature.2020. Doi: 10.1038/d41573-020-00073-5
Conexion Megalabs - Nota Vacunas
Se descubre el primer anticuerpo de origen humano contra SARS-CoV-2
La pandemia ocasionada por SARS-CoV-2 ha generado que gran parte de la comunidad científica se avoque al descubrimiento de anticuerpos capaces de reconocer y neutralizar al virus. La búsqueda de nuevos anticuerpos eficaces contra SARS-CoV-2 tiene un rol crucial en la lucha contra la pandemia, y se suma a los esfuerzos para obtener una vacuna efectiva.
En el año 2003 surgió la pandemia con el virus SARS-CoV, que comparte aproximadamente el 70% de la secuencia genética con el virus SARS-CoV-2. Diversos anticuerpos capaces de neutralizar dicho virus fueron hallados, pero dado que no existían casos desde el año 2004, no se avanzó con sus análisis. En ese entonces se había descubierto que el anticuerpo monoclonal CR3022 era capaz de neutralizarlo a través de su unión con la proteína espiga viral. Recientemente se descubrió que dicho anticuerpo es capaz de neutralizar a SARS-CoV-2 al unirse a la proteína espiga del mismo, presente en la envoltura viral y que homóloga a la proteína espiga de SARS-CoV. Este anticuerpo tiene una característica particular, y es que no compite con el sitio de unión a la célula del receptor celular ACE2 (enzima convertidora de angiotensina I-2; como ocurre con otros anticuerpos), sino que impide estéricamente la unión entre el virus y el receptor ACE2, al unirse con la proteína espiga. Por tanto, este anticuerpo es un “neutralizante cruzado” que reconoce a los virus SARS-CoV y SARS-CoV-2. (1)
Actualmente se han tomado anticuerpos policlonales presentes en el suero de pacientes recuperados para Covid-19, para tratar la infección con SARS-CoV-2. Wang y colaboradores realizaron experimentos utilizando suero con anticuerpos de ratones transgénicos inmunizados. La muestra analizada poseía 51 hibridomas SARS-S que codificaban para inmunoglobulinas quiméricas rata: humano (cadena pesada variable humana, y cadena liviana y región constante de rata). De los 51 hibridomas analizados por la técnica ELISA, se vio que el anticuerpo quimérico 47D11-H2L2 tenía capacidad neutralizante cruzada SARS-CoV y SARS-CoV-2. Este candidato fue rediseñado hacia una composición completamente humana, al clonar la cadena pesada variable y la cadena liviana de una IgG humana. Este anticuerpo modificado biotecnológicamente, denominado 47D11, fue utilizado en posteriores análisis en células VeroE6 infectadas con ambos tipos de virus. Los resultados demostraron que el anticuerpo monoclonal 47D11 es capaz de inhibir potentemente la infección de virus SARS-Cov y SARS-CoV-2 en el cultivo celular estudiado, a través de un mecanismo aún no elucidado completamente, pero diferente al mecanismo empleado por otros anticuerpos como el impedimento estérico. El mecanismo probable planteado por los autores establece que es probable que la interacción con la proteína espiga genere la desestabilización viral y la perfusión de la estructura del virus. (2)
Se espera que se sigan descubriendo nuevos anticuerpos humanos contra SARS-CoV-2 y que sean sometidos a estudios in vitro e in vivo para demostrar la capacidad neutralizante (estudios preclínicos); y que posteriormente demuestren su eficacia en estudios clínicos.
Bibliografía:
2- Wang C et al. A human monoclonal antibody blocking SARS_CoV-2 infection. Nature. 2020. 11, 2251.
Conexion Megalabs -Se descubre el primer anticuerpo de origen humano contra SARS-CoV-2

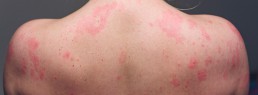
COVID19 y lesiones dermatológicas
El presente material se presenta exclusivamente con fines informativos y de formación para el cuerpo médico.
COVID-19 puede afectar diferentes sistemas y órganos, incluyendo la piel. Hay pocas descripciones de las manifestaciones cutáneas de COVID-19. El veinte por ciento de los pacientes de una sala médica italiana tenían lesiones cutáneas, descritas como erupción cutánea, urticaria o un caso de lesiones «similares a la viruela». Otros informes de casos describen una erupción confundida con dengue, acro-isquemia en niños y pacientes críticos, placas en los talones y urticaria. La mayoría de estos informes carecen de imágenes clínicas, debido a problemas de seguridad, y describen pocos pacientes en entornos hospitalarios. No existe una clasificación previa y detallada ni una descripción de las manifestaciones cutáneas de COVID-19.
Esta información puede resultar útil para manejar a los pacientes, reconocer a los pacientes con pocos síntomas y proporcionar información de pronóstico. El reconocimiento de pacientes paucisintomátcos también podría ser útil para el control epidemiológico, especialmente en áreas donde las pruebas diagnósticas son escasas. Por todas estas razones, realizamos una encuesta de recolección de casos dermatológica a nivel nacional, para describir rápidamente las manifestaciones cutáneas de la enfermedad COVID-19 y relacionarlas con otros trastornos clinicos.
atlas lesiones covid BJD
FDA aprueba dos medicamentos genéricos que facilitan la intubación traqueal
Debido a que la pandemia de COVID-19 produjo un aumento del ingreso de pacientes en la unidad de cuidados intensivos, en donde la mayoría de los enfermos críticos requieren ventilación mecánica, el 04 de mayo de 2020 la Administración de Alimentos y Medicamentos de EE. UU (FDA) aprobó dos medicamentos genéricos indicados para facilitar la intubación traqueal y proporcionar relajación del músculo esquelético durante la cirugía o la ventilación mecánica: el cloruro de succinilcolina USP 200 mg / 10 ml inyectable y el besilato de cisatracurio USP 20 mg / 10 ml inyectable. (1)
El cloruro de succinilcolina (relajante del músculo esquelético despolarizante, de acción ultracorta) fue aprobado por la FDA en el año 1952 (2) y por la Agencia Española de Medicamentos y Productos Sanita-rios (AEMPS) en 1960 (3), y el besilato de cisatracurio (relajante del músculo esquelético no despolari-zante, de acción intermedia) en el año 1995 y 1996 por la FDA (4) y AEMPS (5) respectivamente.
(1) Food and Drug Administration (FDA). Coronavirus (COVID-19) Update. Disponible en:
https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-daily-roundup-may-5-2020
(2) Food and Drug Administration (FDA). FDA Approved Drugs_Succinylcholine chloride. Dis-ponible en:
https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=008453
(3) Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). AEMPS Autorización del producto_Succinilcolina cloruro. Disponibile en:
https://cima.aemps.es/cima/publico/detalle.html?nregistro=33815
(4) Food and Drug Administration (FDA). FDA Approved Drugs_ Cisatracurium besyate. Dispo-nible en:
https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=020551
(5) Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). AEMPS Autorización del producto_ Cisatracurio besilato. Disponibile en:
https://cima.aemps.es/cima/publico/detalle.html?nregistro=61200
Autoridad Sanitaria_FDA FINAL
FDA autoriza el uso de emergencia de Remdesivir como posible tratamiento de COVID-19
El 01 de mayo de 2020 la Administración de Alimentos y Medicamentos de EE. UU (FDA) emitió la autorización para el uso de emergencia (EUA, por su sigla en inglés) del fármaco antiviral en investigación Remdesivir, para el tratamiento de COVID-19 en adultos y niños hospitalizados con enfermedad grave.
La autorización de uso de emergencia permite que Remdesivir se distribuya en los EE. UU. y se otorgue a los proveedores de atención médica para ser utilizado en pacientes como tratamiento de la infección por COVID-19 sospechoso o confirmado por laboratorio, utilizando la vía intravenosa para su administración. El uso estará dirigido a aquellos pacientes con niveles bajos de oxígeno en la sangre que necesitan terapia con oxígeno o soporte respiratorio más intensivo como ventilación mecánica.
Si bien existe información limitada sobre la seguridad y la eficacia del uso de Remdesivir en el tratamiento de pacientes hospitalizados con COVID-19, se demostró en un ensayo clínico que el fármaco en investigación acorta el tiempo de recuperación en algunos pacientes.
Con base en la evaluación de los criterios de autorización de uso de emergencia y la evidencia científica disponible, se determinó que es razonable creer que Remdesivir puede ser eficaz en el tratamiento de COVID-19 y que, dado que no existen tratamientos alternativos adecuados, aprobados o disponibles, los beneficios conocidos y potenciales para tratar este virus grave o potencialmente mortal superan actualmente los riesgos conocidos y potenciales del uso del medicamento.
La autorización de uso de emergencia implica que la información importante sobre el uso de Remdesivir en el tratamiento de COVID-19 se ponga a disposición de los proveedores de atención médica y pacientes, incluidas las instrucciones de dosificación, los posibles efectos secundarios y las interacciones con otros medicamentos. Los posibles efectos secundarios de Remdesivir incluyen: aumento de los niveles de enzimas hepáticas, que pueden ser un signo de inflamación o daño a las células del hígado; y reacciones relacionadas con la perfusión, que pueden incluir presión arterial baja, náuseas, vómitos, sudoración y escalofríos.
La emisión de una autorización de uso de emergencia está destinada a proporcionar disponibilidad de un medicamento durante una emergencia; una EUA no es el equivalente a una aprobación de la FDA. Al determinar si se debe emitir una EUA, la FDA evalúa la evidencia disponible y coteja cuidadosamente los riesgos conocidos o potenciales de un fármaco no probado con aquellos beneficios conocidos o potenciales para ponerlo a disposición durante la emergencia.
Texto tomado de:
https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-issues-emergency-use-authorization-potential-covid-19-treatment
Autoridad Sanitaria_FDA Remdesivir final
Pelargonium sidoides
EPs® 7630 es la sustancia activa de los productos medicinales conteniendo extracto acuoso etanólico de raíces de Pelargonium sidoides. La fecha de nacimiento internacional (IBD, International Birth Date) de las preparaciones conteniendo EPs® 7630 es 10 de diciembre del 2005, cuando la autorización de la comercialización fue otorgada en Alemania.
Esta formulación en comprimidos se encuentra registrada en más de 20 países de Europa, Latinoamérica y Asia (UK Medicine and Healthcare Regulatory Agency 2009).
Este extracto tiene propiedades antibacterianas, antivirales e inmunomoduladoras.
Está indicado para el tratamiento de infecciones agudas y crónicas principalmente de las vías respiratorias y de la zona de oídos, nariz y garganta, por ejemplo: bronquitis, sinusitis, amigdalitis y rinofaringitis. Contribuye a prevenir sobreinfecciones bacterianas en enfermedades virales. (1-5)
Los resultados de los ensayos clínicos muestran que el extracto de Pelargonium sidoides es eficaz y seguro en el tratamiento iinfecciones respiratorias tales como resfriado común y bronquitis aguda, reduciendo significativamente la gravedad y duración de los síntomas en comparación con el placebo. (6)
Las especies de Pelargonium investigadas hasta la fecha contienen una proporción relativamente alta de taninos y diversas cantidades de derivados cumarínicos, flavonoides, esteroles, aminas y aminoácidos. Los taninos y las cumarinas (derivados de la 7-hidróxicumarina) son los componentes activos principales contenidos en el extracto de Pelargonium sidoides, que se consideran que influyen en la eficacia.
Posee un mecanismo de acción multifactorial. El extracto EPs® 7630 ha demostrado varios efectos in vitro que son relevantes para el uso clínico, en particular, la estimulación de los mecanismos de defensa inespecíficos, efectos antimicrobianos directos e indirectos, así como propiedades citoprotectoras. En ensayos animales con ratones, la administración oral de EPs® 7630 provocó una inhibición del comportamiento de la enfermedad (síntomas inespecíficos de la enfermedad durante enfermedades infecciosas). En los ratones infectados con virus influenza la inhalación de EPs® 7630 condujo a una mejora significativa de la tasa de supervivencia, así como la temperatura y el peso corporal.
En modelos animales, la administración oral de EPs® 7630 redujo significativamente la frecuencia de la tos y prolongó el tiempo de latencia de la tos, de forma dosis-dependiente. Además, el extracto de EPs® 7630 ejerce una actividad secretolítica marcada. Los cambios histopatológicos debido a la bronquitis aguda bacteriana se redujeron significativamente en ratas tratadas con EPs® 7630. Este efecto protector parece estar mediada (al menos parcialmente) por una regulación de la superóxido dismutasa y posteriormente a un efecto protector contra el estrés oxidativo.
Propiedades antivirales y citoprotectoras.
El efecto citoprotector de Pelargonium sidoides y sus diferentes componentes sobre la destrucción celular inducida por los virus se confirmó con el siguiente modelo: fibroblastos que fueron incubados con residuos de macrófagos (inducción de interferón por la sustancia de control/EPs ® 7630) e infectados con el virus de la encefalomiocarditis (EMCV).
Pelargonium sidoides también aumenta la liberación de péptidos antimicrobianos de los granulocitos neutrófilos, las llamadas defensinas.
Las defensinas fueron descubiertas inicialmente en las plantas, que, a diferencia de los mamíferos, no tienen sistema inmunológico específico, y que se han defendido con éxito por millones de años contra el ataque de microorganismos en un medio con una carga de patógenos muy alta, como es el suelo. En los seres humanos, las defensinas, entre otros, se han detectado en la superficie de células CD4 en la piel. Se dice que estas juegan un papel esencial en la defensa contra agentes patógenos.
El extracto de Pelargonium sidoides es efectivo contra una variedad de virus respiratorios incluyendo virus de la gripe A (H1N1, H3N2), Coxsackie A9, Coronavirus, Virus sincicial respiratorio, parainfluenza virus 3. (26)
Inmunomodulación.
El efecto antiviral de Pelargonium sioides se deriva principalmente de la modulación sobre el sistema inmune no específico. Pelargonium sioides desencadena la estimulación de la síntesis de interferón (INF- β). Esto es particularmente relevante debido a que el interferón tipo 1 INF- β como citoquina no sólo protege a las células contra la destrucción por los virus, sino también
tiene un efecto antiviral directo y activa a las células natural killer. Esta última juega un papel importante en las etapas iniciales de la infección como células inmunes en la primera línea de defensa.
Un estudio llevado a cabo con EPs ® 7630 en cultivos de células humanas utilizando el dsRNA viral análogo polyl: poliC confirma este efecto. (7)
Además, Pelargonium sidoides induce otros interferones del tipo 1, el IFN- α y el INF-γ que también poseen propiedades citoprotectoras. (15)
Mejora de la función fagocitaria.
El aumento de la fagocitosis y la destrucción intracelular de los microorganismos (la muerte intracelular) es otra de las propiedades farmacológicas con las que cuenta Pelargonium para cortar el curso de una infección. Una mejora significativa en la función de los fagocitos humanos se detectó en los ensayos de citometría de flujo correspondientes utilizando Candida albicans como organismo objetivo. (8,9)
Propiedades anti-bacterianas.
En un estudio llevado a cabo con cepas multirresistentes de Staphylococcus aureus (MRSA), la susceptibilidad de estas cepas a Pelargonium sidoides era favorable en comparación con la cepa de referencia no resistente, St. aureus ATCC 2592336. (10)
Propiedades secretomotoras.
Al aumentar el transporte de agentes patógenos y mucus de las vías respiratorias, el conteo de patógenos se reduce y el medio nutritivo para su posterior proliferación se elimina, todo esto favorece para que la respiración mejore sustancialmente.
Pelargonium sidoides reduce la carga de patógenos. De esta manera, protege contra la colonización bacteriana, la infección, la sobreinfección y la recurrencia.
Dosis y administración
La vía de administración de Pelargonium es oral, se recomienda tomar la dosis antes de las comidas con abundante líquido y sin masticar el comprimido.
Niños entre 6 y 12 años
Tomar un comprimido cada 12 horas. Se desaconseja el uso de los comprimidos en menores de 6 años ya que puede ser dificultoso su uso en este grupo etareo, para ello se dispone de la presentación de Pelargonium sidoides en forma de gotas.
Adolescentes mayores de 12 años y adultos: un comprimido cada 8 horas.
Precauciones y advertencias
En el prospecto se recomienda al paciente consultar en breve con un médico, si la condición clínica no mejora en una semana, en caso de que la fiebre dure por varios días o si se tiene dificultad para respirar o esputos con sangre.
Embarazo
No existe evidencia de acción teratogénica. Sin embargo, por carecer de suficiente experiencia, se sugiere no administrar en embarazo y lactancia.
Eventos adversos
Con muy baja frecuencia pueden ocurrir molestias gastrointestinales (náuseas y vómitos).
En raras ocasiones, se han observado sangrado leve de encías y nariz, reacciones de hipersensibilidad.
Muy raro: disfunción hepática, la relación causal entre estos hallazgos y el uso de este medicamento no ha sido demostrada.
Estudios clínicos
La eficacia y seguridad del extracto EPs 7630 en el tratamiento de infecciones agudas del tracto respiratorio ha sido estudiada en más de 3.500 pacientes en estudios clínicos controlados por placebo, doble ciego, y en más de 5.500 pacientes en estudios de etiqueta abierta y no intervencionistas (vigilancia después de la comercialización). De un total de más de 9.000 pacientes, alrededor de 4.000 eran niños y adolescentes.
Referencias bibliográficas
1. Agbabiaka, T.B., Guo, R. & Ernst, E. (2008). Pelargonium sidoides for acute bronchitis: a systematic review and meta-analysis. Phytomedicine. Vol. 15, No. 5, pp. 378-385
2. Brown, D. (2009). Pelargonium sidoides extract (EPs 7630): alternative treatment of acute upper respiratory tract infections. Natural Medicine Journal, Vol. 1, No. 4, pp. 1-6
3. Chuchalin, A.G., Berman, B. & Lehmacher, W. (2005). Treatment of acute bronchitis in adults with a Pelargonium sidoides preparation (EPs® 7630): a randomized, dou-ble-blind, placebo-controlled trial. Explore, Vol. 1, No. 6, pp. 437-445
4. Franks, P. & Gleiner, J.A. (1984). The treatment of acute bronchitis with trime-thoprim and sulfamethoxazole. The Journal of Family Practice, Vol. 19, No. 2, pp. 185-190
5. Index nominum: International Drug Directory – Pelargonium sidoides – Edited by the Swiss Pharmaceutical Society. ©2015. Medpharm Scientific Publishers, Stuttgart, Germany Licensed through Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart, Germany. Copyright © 2015 Truven Health Analytics Inc. All rights reserved.
6. Kamin, W., Maydannik, V.G., Malek, F.A. & Kieser, M. (2010). Efficacy and toler-ability of EPs 7630 in patients (aged 6-18 years old) with acute bronchitis: a randomized, double-blind, placebo-controlled clinical dose-finding study. ActaPaediatrica, Vol. 99, No. 4, pp. 537-543
7. Bao Y; Gao Y; Koch E; Pan X; Jin Y; Cui X. Evaluation of pharmacodynamic activities of EPs® 7630, a special extract from roots of Pelargonium sidoides, in animals models of cough, secretolytic activity and acute bronchitis. Phytomedicine 2015;22(4):504-509.
8. Conrad A et al.: Extract of Pelargonium sidoides (EPs® 7630) improves phagocytosis, oxidative burst, and intracellular killing of human peripheral blood phagocytes in-vitro, Phytomedicine 2007; 14 (Suppl. VI): 46–51.
9. Conrad A et al.: Extract of Pelargonium sidoides (EPs®7630) inhibits the interactions of group A streptococci and host epithelia in vitro, Phytomedicine 2007; 14 (Suppl. VI): 52–59.
10. Kolodziej H, Schulz V: Umckaloabo – von der traditionellen Anwendung zum modernen Phytopharmakon, DAZ 2003; 143: 1303–1312
11. Neugebauer P et al.: A new approach to pharmacological effects on ciliary beat frequency in cell cultures – exemplary measurements under Pelargonium sidoides extract, Phytomedicine 2005; 12: 47–52.
12. Kayser O, Kolodziej H. Antibacterial activity of extracts and constituents of Pelargonium sidoides and Pelargonium reniforme. Planta Med. 1997 Dec; 63(6):508-10.
13. Knutson, D. & Braun, C. (2002). Diagnosis and management of acute bronchitis. American Family Physician, Vol. 65, No. 10, pp. 2039-2044
14. Koch K. Report antioxidative properties of Pelargonium sidoides DC .2001 Internal document
15. Koch E, Lanzendörfer-Goossens H, Wohn C. Stimulation of interferon (INF)-b-synthesis and natural killer (NK) cell activity by an aqueous-ethanolic extract from roots of Pelargonium sidoides (Umckaloabo). Naunyn-Schmeideberg Arch Pharma-col. 2002; 365(Suppl 1):R75 (Abstract 288).
16. Koch K. Evaluation of the contribution of different constituens to the pleotropic pharmacological effects of the special Pelargonium sidoides root extract EPs 7630 .2004 Internal document
17. Kolodziej H, Schulz V: Umckaloabo – von der traditionellen Anwendung zum modernen Phytopharmakon, DAZ 2003; 143: 1303–1312.
18. Macfarlane, J., Holmes, W., Gard, P., Thornhill, D., Macfarlane, R. & Hubbard, R. (2002). Reducing antibiotic use for acute bronchitis in primary care: blinded, random-ised controlled trial of patient information leaflet. British MedicalJournal, Vol. 324, No. 7923, pp. 91-94
19. MARTINDALE – Pelargonium sidoides – The Complete Drug Reference. © The Royal Pharmaceutical Society of Great Britain 2015 © 2015 Truven Health Analytics Inc.
20. Matthys, H., Lizogub, V.G., Malek, F.A. & Kieser, M. (2010b). Efficacy and tolerability of EPs 7630 tablets in patients with acute bronchitis: a randomised, doubleblind, placebo-controlled dose finding study with a herbal drug preparation from Pelargonium sidoides. Current Medical Research and Opinion. Vol. 26, No. 6, pp. 1413-1422
21. Micromedex. Drugdex Evaluations. – Pelargonium sidoides – Last Modified: 2015 © 2015 Truven Health Analytics Inc
22. Neugebauer P et al. A new approach to pharmacological effects on ciliary beat frequency in cell cultures – exemplary measurements under Pelargonium sidoides extract. Phytomedicine 2005; 12: 47–52.
23. Nöldner M, Schötz K. Inhibition of Lipopolysaccharid-Induced Sickness Behaviour by a Dry Extract from the Roots of Pelargonium Sidoides (EPs® 7630) in Mice, Phytomedicine 2007; 14 (Suppl. VI): 27–31.
24. Poisindex® Managements – Plants Pelargonium – 2015 © 2015 Truven Health Ana-lytics Inc.
25. Timmer A, Günther J, Rücker G, Motschall E, Antes G, Kern WV.Cochrane Database Syst Rev. Pelargonium sidoides extract for acute respiratory tract infections. 2008 Jul 16;(3):CD006323. doi: 10.1002/14651858.CD006323.pub2.
26. Tte.1°(QF) Shirley Aquinesa, Tte.1°(QF) Tania Tassanob. Efecto del extracto de Pelargonium sidoides en enfermedades del tracto respiratorio alto y en la respuesta inmunológica. Laboratorio Farmacéutico de la Dirección Nacional de Sanidad de las Fuerzas Armadas (D.N.S.FF.AA.). Servicio de Bromatología de la D.N.S.FF.AA.
Insertos
Conexion Pelargonium sidoides
FDA aprueba Remdesivir como tratamiento para Covid-19
Desde el surgimiento de la pandemia diversos pacientes han sido tratados con Remdesivir (de Gilead Sciences Inc.) para lidiar con la infección de SARS-CoV-2. Estudios pre-clínicos en monos demostraron su eficacia en el tratamiento de esta infección, y su tratamiento ha sido parte de numerosos estudios clínicos que ya están mostrando sus nuevos resultados.
El 10 de abril Grein y colaboradores publicaron los primeros resultados de estos estudios, donde de un total de 53 pacientes se vio que la incidencia acumulada de mejora clínica a los 28 días de seguimiento fue de un 84%. Sin embargo, estos resultados fueron preliminares, y requerían entonces de estudios en mayor número de pacientes para ser confirmados.
Recientemente, el 29 de abril, el Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAID por sus siglas en inglés) ha reportado nuevos resultados favorecedores para el uso de Remdesivir. Este estudio, llamado ACTT: Ensayo de Tratamiento Adaptativo Covid-19 fue el primer estudio de Estados Unidos sobre Covid-19, comenzando el 21 de febrero de 2020. En este estudio controlado por placebo, randomizado y ciego participaron 1063 pacientes. Los resultados preliminares muestran que el uso de Remdesivir logra acelerar los tiempos de recuperación en un 31% (p<0.001), ya que los pacientes que recibieron placebo tardaron en recuperarse 15 días; mientras que los pacientes que recibieron tratamiento con Remdesivir se recuperaron en 11 días. La mortalidad también fue evaluada en este estudio y se observó que en el grupo de tratamiento fue de 8%, mientras que para el grupo placebo fue de 11.6% (p=0.059).
Los resultados detallados serán publicados próximamente; pero los resultados publicados previamente por Grein y Colaboradores y recientemente por NIAID, han despertado el interés de la Agencia de Administración de Comidas y Drogas (FDA) de Estados Unidos. Tanto es así que el 1° de Mayo la FDA anunció la aprobación de emergencia del uso potencial de Remdesivir para tratamiento de Covid-19. Esta aprobación tuvo lugar teniendo en consideración que SARS-CoV-2 causa una enfermedad seria o que pone en riesgo la vida, que no hay una alternativa aprobada y adecuada para esta enfermedad, y a su vez teniendo en consideración la totalidad de la evidencia científica que sugiere que Remdesivir es efectivo para el tratamiento de Covid-19. FDA ha estado en comunicación constante con Gilead Sciences para lograr que este tratamiento esté disponible tan pronto sea posible.
Bibliografía:
– Grein J et al. Compassionate Use of Remdesivir for Patients with Severe Covid-19. The New England Journal of Medicine. 2020. Doi: 10.1056/NEJMoa2007016
– NIAID. NIH Clinical Trial Shows Remdesivir Accelerates Recovery from Advances COVID-19. 2020.
Conexion Megalabs - FDA aprueba Remdesivir como tratamiento para Covid-19

HOSPITAL UNIVERSITARIO FUNDACIÓN JIMÉNEZ DÍAZ
El hospital Universitario Fundación Jiménez Diaz, elaboró un protocolo de tratamiento de la Neumonitis de los pacientes con infección por COVID-19 al ingreso de la hospitalización.
El 23 de marzo 2020 se publica este protocolo que contempla diferentes opciones terapéuticas que van desde antimicrobianos, corticoides e inmunosupresores como la ciclosporina.
Protocolo disponible en:
http://www.ibima.eu/wp-content/uploads/2020/03/Manejo-COVID-19-HOSPITALIZACION-HUFJD_20200323-1.pdf-1.pdf-1.pdf-1.pdf-1.pdf
Conexion Megalabs -Protocolo Jimenez Diaz
Famotidina
La Famotidina fue aprobada en 1997 en Estados Unidos para el tratamiento a corto plazo de la úlcera duodenal activa; terapia de mantenimiento para pacientes con úlcera duodenal a dosis reducidas después de la curación de una úlcera activa; tratamiento a corto plazo de la úlcera gástrica benigna activa; tratamiento a corto plazo de la enfermedad por reflujo gastroesofágico (ERGE) y el tratamiento de afecciones hipersecretoras patológicas (p. Ej., Síndrome de Zollinger-Ellison, endocrina múltiple adenomas).(1,2)
Estudios clínicos con COVID-19
Northwell Health en Nueva York se encuentra actualmente realizando un estudio clínico respecto al uso de Famotidina en COVID-19. El 7 de abril del 2020, los primeros pacientes ingresaron en el hospital de Northwell Health, donde se les administró famotidina por vía intravenosa.
La dosis empleada es unas 9 veces más alta que la dosis usual como antiácido, estimando 40 mg por vía oral y 20 mg para la vía intravenosa, dos veces por día en ambos casos. Los brazos del estudio se componen por pacientes con administración de Famotidina e Hidroxicloroquina por un lado, y pacientes recibieron únicamente Hidroxicloroquina en el brazo control. El estudio tiene el objetivo de estudiar 1174 pacientes.
Reportes de China y modelos moleculares sugieren que este fármaco se une a una encima del virus SARS-CoV llamada proeasa papaino-símil. En una revisión china de 6212 pacientes COVID-19 positivos hospitalizados, se vio que los pacientes con Famotidina tuvieron una tasa de mortalidad de 14%, en comparación con una tasa de 27% para los pacientes que no recibían dicho medicamento, aunque la diferencia no fue estadísticamente significativa. (3)
Dosis y administración propuestas para COVID-19 (3)
En el estudio siendo llevado a cabo por FDA y BARDA en Northwell Health en Nueva York y mencionado más adelante, la dosis empleada es unas 9 veces más alta que la dosis usual como antiácido, estimando 40 mg por vía oral y 20 mg para la vía intravenosa, dos veces por día en ambos casos. (3)
Precauciones y advertencias (2)
Dado que se han informado efectos adversos del SNC en pacientes con insuficiencia renal moderada y grave, puede ser necesario utilizar intervalos más largos entre dosis o dosis más bajas en pacientes con moderado (aclaramiento de creatinina <50 mL/min) o insuficiencia renal grave (aclaramiento de creatinina <10 ml / min).
Lactancia
Los estudios realizados en ratas lactantes han demostrado que la famotidina se secreta en la leche materna. Debido a la posibilidad de serias reacciones adversas en lactantes, se debe tomar la decisión de suspender la lactancia o suspender el medicamento, teniendo en cuenta la importancia del medicamento para la madre.
Eventos adversos (2)
Se ha informado que las siguientes reacciones adversas ocurren en más del 1% de los pacientes en tratamiento con Famotidina en ensayos clínicos controlados, y puede estar causalmente relacionado con el medicamento: dolor de cabeza (4.7%), mareos (1.3%), estreñimiento (1.2%) y diarrea (1.7%).
Las siguientes otras reacciones adversas se han informado con poca frecuencia
• Cuerpo en general: fiebre, astenia, fatiga.
• Cardiovascular: arritmia, bloqueo AV, palpitación
• Gastrointestinales: ictericia colestática, anomalías de las enzimas hepáticas, vómitos, náuseas, molestias abdominales, anorexia, boca seca
• Hematológicos: casos raros de agranulocitosis, pancitopenia, leucopenia, trombocitopenia.
• Hipersensibilidad: anafilaxia, angioedema, edema orbitario o facial, urticaria, erupción cutánea, inyección conjuntival.
• Musculoesquelético: dolor musculoesquelético incluyendo calambres musculares, artralgia.
• Sistema nervioso/psiquiátrico: convulsiones de gran mal; trastornos psíquicos, que eran reversibles en casos de qué seguimiento se obtuvo, incluyendo alucinaciones, confusión, agitación, depresión, ansiedad, disminución libido; parestesia; insomnio; somnolencia. Las convulsiones, en pacientes con insuficiencia renal, han sido reportado muy raramente.
• Respiratorio: broncoespasmo, neumonía intersticial
• Piel: necrólisis epidérmica tóxica / síndrome de Stevens Johnson (muy raro), alopecia, acné, prurito, piel seca, rubor
• Otros: tinnitus, trastorno del gusto, se han informado casos raros de impotencia y casos raros de ginecomastia
(1) Food and Drug Administration (FDA). FDA Approved Drugs. Disponible en:
https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=020249
(2) Inserto Pepcid. Food and Drug Administration. 2007. Disponible en:
https://www.accessdata.fda.gov/drugsatfda_docs/label/2007/019462s034,019510s031,020249s013lbl.pdf
(3) Brendan Borrell. New York clinical trial quietly tests heartburn remedy against coronavirus. 26 de abril del 2020. Disponible en:
https://www.sciencemag.org/news/2020/04/new-york-clinical-trial-quietly-tests-heartburn-remedy-against-coronavirus
Conexion Famotidina Inyectable