AstraZeneca espera que el mundo pueda centrarse en sus noticias positivas sobre vacunas
CNN-Actualizado a 0956 GMT (1756 HKT) 27 de noviembre de 2020
Cuando la farmacéutica británico-sueca AstraZeneca anunció el lunes que su vacuna experimental contra el coronavirus tiene una efectividad del 70% en promedio, el mundo exhaló un suspiro colectivo de alivio y las acciones se recuperaron. Había llegado otra vacuna con resultados prometedores.
Pero la falta de claridad en torno a varios aspectos de los datos de los ensayos de la vacuna de AstraZeneca ha despertado algunas dudas en la comunidad científica, lo que podría retrasar el momento de la autorización de la vacuna en Europa y EE. UU.
AstraZeneca dijo el lunes que los participantes del estudio en el Reino Unido habían recibido dos dosis diferentes de la vacuna.
El fabricante de medicamentos, que desarrolló la vacuna con la Universidad de Oxford, sin embargo, en ese momento, no explicó por qué usaron dos regímenes de dosificación diferentes o por qué el tamaño de un grupo era significativamente menor que el del otro.
En un grupo, 2.741 participantes recibieron media dosis de la vacuna y luego una dosis completa al menos un mes después. Este grupo estaba protegido en un 90% contra Covid-19.
En el segundo grupo, 8.895 participantes recibieron una dosis completa seguida de otra dosis completa al menos un mes después. Este grupo solo estaba protegido en un 62%.
Es por eso que AstraZeneca dice que su vacuna tiene una efectividad del 70%, en promedio.
Pero algunos científicos se preguntan por qué la empresa informaría sobre un resultado combinado de dos ensayos diferentes, ya que se desvía de los informes estándar sobre ensayos clínicos.
Y en los días posteriores a ese anuncio, ha surgido otro punto de confusión.
El martes, Menelas Pangalos, vicepresidente ejecutivo de AstraZeneca que dirige la investigación y el desarrollo no oncológicos, explicó por primera vez a Reuters que un error de laboratorio era la razón por la que algunos voluntarios habían recibido una dosis más pequeña, la dosis que resultó ser 90% efectiva. «La razón por la que recibimos la mitad de la dosis es la casualidad», dijo Pangalos, y agregó que los investigadores «habían sub-dosificado la dosis de la vacuna a la mitad».
En un comunicado el miércoles, el gerente de comunicaciones de Oxford para vacunas le dijo a CNN que «la selección de la dosis para cualquier nueva vacuna es un área complicada, y al explorar los métodos de selección de la dosis, descubrimos que una grupo recibió una dosis más baja de la esperada».
Oxford elaboró más el jueves, diciendo en un comunicado a CNN que una «diferencia en el proceso de fabricación» había llevado al error.
Ese problema de fabricación se ha corregido desde entonces, dice el comunicado, señalando que el regulador del Reino Unido que supervisa la prueba había acordado incluir «ambos enfoques» en la Fase 3.
Si bien AstraZeneca y Oxford enfrentan críticas por la transparencia, dado que no mencionaron el error en su comunicado de prensa que anuncia los resultados ni en una llamada de prensa el lunes, la compañía cree que el mundo debería centrarse en los resultados positivos de la prueba.
En declaraciones al Wall Street Journal el miércoles, el vicepresidente ejecutivo de AstraZeneca dijo: «El error es realmente irrelevante. Independientemente de la forma en que corte los datos, incluso si sólo cree en los datos de dosis completa, todavía tenemos una eficacia que cumple con los umbrales de aprobación con una vacuna que tiene una efectividad superior al 60%», dijo Pangalos, según el Wall Street Journal.
AstraZeneca y Oxford aún tienen que presentar un candidato para una entrevista al aire, según lo solicitado por CNN.
La Administración de Drogas y Alimentos de EE. UU. requiere un umbral de eficacia de al menos el 50%. Sin embargo, no está claro si la FDA autorizará el uso de emergencia.
AstraZeneca aún no ha probado su dosis media en los EE. UU. tampoco. Pero el jueves, un portavoz de la compañía le dijo a CNN que su objetivo era incluir el régimen de dosis de media potencia en sus ensayos en EE. UU., que actualmente tienen alrededor de 10,000 participantes.
El portavoz dijo que la compañía espera reclutar alrededor de 40.000 voluntarios en total, algunos de los cuales recibirán la vacuna de media dosis. Agregaron que estaban en «discusiones en curso» con la FDA para su aprobación, y agregaron que no se había anunciado nada formal.
El lunes, el Dr. Paul Offit, miembro del Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA, que revisará las vacunas Covid-19 antes de que salgan al mercado, dijo que la falta de datos que los llevó a sus conclusiones hizo es «difícil conocer el significado de sus hallazgos».
Cuando otros dos importantes fabricantes de medicamentos, Pfizer y Moderna, publicaron sus resultados de eficacia a principios de este mes, sí incluyeron los datos que llevaron a sus resultados.
AstraZeneca presentó un análisis de 23.000 participantes en su ensayo de fase 3.
Dijo que algunos participantes recibieron la vacuna Covid-19, mientras que otros recibieron una vacuna diferente para un virus no relacionado o inyecciones de placebo.
Un total de 131 participantes del estudio desarrollaron Covid-19, dijo AstraZeneca, pero no dijeron cuántas de esas personas habían recibido la vacuna.
Lo que tampoco está claro es por qué los regímenes de dos dosis produjeron medidas de eficacia tan diferentes.
El investigador principal del ensayo en Oxford, el profesor Andrew Pollard, dijo a los periodistas el lunes que es probable que tenga que ver con el delicado equilibrio de dosificar a alguien lo suficiente para desencadenar una respuesta inmune contra la enfermedad.
«Lo que siempre hemos intentado hacer con una vacuna es engañar al sistema inmunológico haciéndole creer que hay una infección peligrosa a la que debe responder, pero haciéndolo de una manera muy segura», explicó Pollard.
Por lo tanto, puede ser que la mejor manera de «poner en acción al sistema inmunológico» sea administrar al cuerpo una pequeña cantidad de la vacuna para empezar, y luego seguir con una cantidad mayor, dijo.
Respondiendo a si tenía una confianza genuina en que el 90% de éxito del grupo de media dosis no era solo una característica de un tamaño de muestra pequeño, Pollard dijo que el resultado fue «muy significativo… incluso con los números que tenemos».
Pero los expertos se preguntan si esos resultados se mantendrán si más personas reciben el régimen de dosis más baja.
En una llamada con los periodistas el miércoles, el zar de las vacunas de EE. UU. Moncef Slaoui dijo que estaban revisando los datos de la vacuna de AstraZeneca.
Dijo que el grupo que recibió la dosis erróneamente más baja que produjo el 90% de eficacia había sido un grupo más joven, sin nadie mayor de 55. Eso podría afectar potencialmente la potencia de los hallazgos de AstraZeneca, dado que los jóvenes suelen producir respuestas inmunes más fuertes a las vacunas.
Tanto Oxford como AstraZeneca le dijeron a CNN el jueves que no pudieron dar un desglose de las edades de las personas que recibieron la vacuna en ese grupo más pequeño.
Un portavoz de AstraZeneca le dijo a CNN el jueves que, «dada la alta eficacia que hemos visto ahora con los diferentes regímenes de dosificación, hay un gran mérito en continuar investigando estos hallazgos para establecer el régimen de dosificación más eficaz para la vacuna».
Agregó que la compañía está teniendo conversaciones con reguladores de todo el mundo para evaluar los hallazgos y que esperan la publicación de resultados revisados por pares.
Pero el Dr. Saad Omer, especialista en vacunas de la Facultad de Medicina de Yale, cree que el grupo con una tasa de eficacia del 90% es relativamente pequeño y es posible que los resultados no se mantengan cuando más personas reciben este régimen.
«Odio criticar a mis compañeros académicos, o a cualquier otra persona», dijo, «pero divulgar información como esta es como pedirnos que intentemos leer las hojas de té».
Las acciones de Astrazeneca han caído más de un 6% desde su anuncio el lunes.
https://edition.cnn.com/2020/11/26/europe/astrazeneca-oxford-vaccine-data-concerns-intl/index.html
vacuna astra zeneca

Asociación Colombiana de Farmacología alerta sobre tratamiento para COVID-19
De forma similar a lo sucedido con otros medicamentos, en la prevención o tratamiento de COVID-19, la N-acetilcisteina es una molécula que aún no cuenta con evidencia suficiente para su uso como profiláctico o preventivo, advierte la Asociación Colombiana de Farmacología
A finales del mes de agosto, la Asociación Colombiana de Farmacología (ASOCOL-FAR) y el Grupo de Investigación en Farmacoepidemiología y Farmacovigilancia de la Universidad Tecnológica de Pereira, emitieron un comunicado a los médicos en general, con las recomendaciones y sobre todo los riesgos que tiene el uso de la N-acetilcisteina en el manejo del COVID-19.
El mensaje principal para la población es no automedicarse, ni dejarse guiar por in-formación acerca de medicamentos que previenen el contagio de COVID-19 ya que por ahora no existe ninguna evidencia científica que lo demuestre.
En el caso del cuerpo médico, se les invita a que evalúen en forma completa toda la información que llega a través de las redes, ya que se están recomendando concentraciones altas de esta molécula que solo se consiguen en administración intravenosa o inhalada y que en forma oral incrementan la posibilidad de presentar eventos adversos importantes.
“Lo que más preocupa es que algunos de los medicamentos que están siendo utilizados erróneamente para manejar o prevenir el COVID-19tienen efectos adversos comprobados y sin embargo, son de venta libre y se consiguen en farmacias y droguerías. Es el caso de la N-acetilcisteina que tiene uso como mucolítico, y cuya utilidad se limita a algunas enfermedades muy específicas. Incluso su uso no está permitido en pacientes menores a 2 años. Se debe usar con precaución en algunas personas por su asociación al aumento de obstrucción de las vías respiratorias (broncoespasmo), por lo que actualmente no se recomienda el uso generalizado de este medicamento ni en el paciente hospitalizado, ni en el paciente ambulatorio, como tratamiento profiláctico o preventivo de la infección por SARS-CoV-2 causante del COVID- 19 hasta que se tenga evidencia que demuestre un beneficio real, teniendo en cuenta sus precauciones y contraindicaciones”, resalta el doctor Jorge Machado, Presidente de la Asociación Colombiana de Farmacología.
ASOCOLFAR evaluó las diferentes moléculas que se han postulado desde el inicio de la pandemia como alternativas de manejo para la COVID-19 haciendo las recomendaciones pertinentes.
Los inhibidores de la enzima convertidora de angiotensina (iECA) y los antagonistas del receptor de angiotensina (ARA2), son medicamentos para tratar la hipertensión arterial (HTA). Análisis sobre el COVID-19 ha mostrado una posible relación entre el uso de estas moléculas y un riesgo aumentado de infección por SARS-CoV-2, “sin embargo, esto no se ha demostrado y sí se sabe que los pacientes con HTA mal controlada tienen peores desenlaces. Por esta razón mientras los estudios no sean concluyentes, se recomienda no suspender, ni cambiar ninguno de estos medicamentos ante la infección por SARS-CoV-2″, dice la asociación.
Por otro lado, los corticoesteroides fueron utilizados durante los brotes del Síndrome Respiratorio Agudo Severo (SARS-CoV-1) y Síndrome Respiratorio del Medio Oriente (MERS-CoV), por lo cual se están utilizando en pacientes con COVID-19 adicionado a otros tratamientos. Sin embargo, la evidencia actual sobre el uso de éstos es controversial.
Aunque los resultados preliminares con respecto al uso de dexametasona son prometedores, aún se está a la espera de la publicación de los resultados finales que permitan concluir con certeza el impacto del uso de esta terapia en pacientes con COVID-19 severos. Por lo que se debe limitar su uso actual a pacientes con ventilación asistida, SDRA, choque séptico, exacerbación de asma o EPOC asociado a la infección por SARS-CoV-2 o que requieren de oxígeno suplementario. No se recomienda su uso en pacientes con infecciones leves o en casa, su uso debe ser siempre bajo supervisión médica por sus efectos secundarios.
El uso de medicamentos como cloroquina, hidroxicloroquina, azitromicina y lopina-vir/ritonavir se basa en resultados positivos en análisis in-vitro es decir en resultados de laboratorio y no con pacientes. Si bien los resultados parecen ser prometedores, se considera que la evidencia actual no es suficiente para recomendar su utilización a gran escala, y mucho menos como terapia profiláctica.
“Dada la cantidad de información a la cual los pacientes actualmente tienen acceso; con base en todos los riesgos ya mencionados y los resultados que aún no son concluyentes para el tratamiento de la infección por COVID-19 con estos medicamentos, es imperativo que los pacientes no se automediquen. El uso de cualquiera de estos medicamentos solo puede hacerse tras la prescripción de un médico con experiencia en el manejo de este tipo de terapias y en un ambiente hospitalario”, dijo el doctor Jorge Machado, presidente de la Asociación Colombiana de Farmacología
Más información:
https://www.elespectador.com/noticias/salud/alerta-sobre-tratamiento-para-covid-19-si-evidencia-suficiente/
Asociación Colombiana de Farmacología alerta sobre tratamiento para COVID-19

La crononutrición analiza la importancia de la hora que comemos y cómo influye sobre nuestro organismo
La crononutrición es una rama de la nutrición que está cobrando cada vez más importancia en todo el mundo.
Almorzar tarde se asocia a mayor riesgo cardiometabólico y peores resultados en la pérdida de peso. Esta es la principal conclusión de un estudio publicado en American Journal of Clinical Nutrition
https://pubmed.ncbi.nlm.nih.gov/33022698/
realizado por un grupo de expertos internacionales dirigidos por la Dra. Marta Garaulet catedrática de Fisiología de la Universidad de Murcia.
En el estudio participó un total de 3.362 personas, la mayoría de ellas de sexo femenino (79,2%), con media de edad de 41 años y obesidad. La variable utilizada fue el punto medio de ingesta que se calcula determinando el punto medio entre la hora de inicio del desayuno y la de finalización de la cena.
En función de este cálculo los participantes se clasificaron en comedores tempranos y los tardíos. Las personas cuyo punto medio de ingesta se situaba después de las 15:00 horas coincidían con aquellas que presentaban índice de masa corporal más elevado al inicio de la investigación. Tenían valores más altos de triglicéridos y menor sensibilidad a la insulina que los comedores tempranos.

La OMS presentó la primera estrategia mundial para eliminar el cáncer de cuello uterino
El objetivo de la OMS es reducir más del 40% de los casos #nuevos de esta enfermedad y 5 millones de muertes asociadas para 2050 a través de la vacunación, detección y tratamiento.
Es la primera vez que 194 países se comprometen a eliminar un tipo de cáncer, tras la adopción de una resolución en la Asamblea Mundial de la Salud de este año
https://www.who.int/news-room/events/detail/2020/11/17/default-calendar/launch-of-the-global-strategy-to-accelerate-the-elimination-of-cervical-cancer
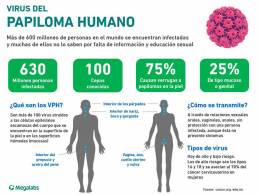
El factor de riesgo más importante del cáncer de cuello uterino es la infección por el virus del papiloma humano VPH. Es una enfermedad prevenible y curable si se detecta y se trata a tiempo. Sin embargo, es el cuarto cáncer más común entre las mujeres a nivel mundial.
La estrategia de la OMS consiste en alcanzar tres objetivos antes de 2030:
- La vacunación en el 90% de las niñas a los 15 años contra el virus del papiloma humano
- Pruebas diagnósticas en el 70% de las mujeres a los 35 años y nuevamente a los 45
- Tratamiento en el 90% de las mujeres identificadas con enfermedad cervical
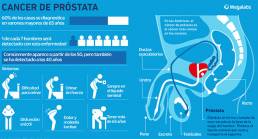
¿Qué es el cáncer de próstata?
La próstata es una pequeña glándula en forma de nuez en los hombres que produce el líquido seminal que nutre y transporta el esperma. El cáncer se origina cuando algunas células en la próstata se vuelven anormales. Las mutaciones en el ADN de células anormales causan que estas crezcan y se dividan de manera más rápida que las células normales.
Generalmente el cáncer de próstata tiene un crecimiento muy lento y su desarrollo se limita a la glándula prostática, por lo que es posible detectarlo a tiempo. Aun así, algunos tipos de cáncer de próstata sí pueden resultar más agresivos y diseminarse con mayor rapidez.
Síntomas más frecuentes:
- Problemas para orinar
- Disminución en la fuerza del flujo de la orina
- Presencia de sangre en el semen
- Molestia en la zona pélvica
- Dolor en los huesos
- Disfunción eréctil
La detección a tiempo es fundamental para evitar su expansión y poder llevar a cabo un tratamiento exitoso que extermine la enfermedad.
Pide una cita con tu médico si tienes algún signo o síntoma que te preocupe.
Moderna manifiesta una efectividad del 94,5% de su vacuna frente al Covid-19
Moderna ha asegurado este lunes que su vacuna experimental es un 94,5% efectiva para prevenir el coronavirus, según los datos provisionales obtenidos del ensayo clínico en etapa avanzada, convirtiéndose así en la segunda compañía estadounidense en una semana en informar resultados que superan las expectativas.
Los datos publicados en una nota de prensa por Moderna implican que el riesgo de enfermar por Covid-19 se redujo en un 94,5% entre el grupo de placebo y el grupo vacunado del ensayo clínico en curso en los Estados Unidos. Los datos clínicos preliminares están basados en el análisis de 95 de los 30.000 voluntarios del estudio fase 3 de la vacuna mRNA-1273 y de la respuesta en cinco personas que recibieron dosis de la vacuna, frente a 90 que sólo recibieron un placebo.
Stéphane Bancel, consejero delegado de la compañía con sede en Massachusetts, anunció que este es un momento crucial en el desarrollo de la vacuna frente a covid-19. Los resultados positivos preliminares del estudio de la fase 3 han dado la primera validación clínica de que la vacuna puede prevenir la enfermedad, incluidos los casos graves», indicó Bancel en un comunicado.
La empresa estadounidense Modrena desarrolla una vacuna en base a tecnología de ARN mensajero y manifiesta una ventaja clave frente a otros desarrollos similares como lo es la no necesidad de almacenamiento ultrafrío, lo que facilitaría su distribución. Moderna espera que la vacuna sea estable a temperatura estándar de los refrigeradores, de 2 a 8 grados Celsius durante 30 días, y que se pueda almacenar hasta 6 meses a -20 grados Celsius.
El siguiente paso que plantea la farmacéutica, será proveer toda la documentación y datos de eficacia de al menos dos meses necesarios para que la Agencia de Alimentos y Medicamentos de Estados Unidos (FDA, en sus siglas en inglés) les conceda la autorización de emergencia, que permite poner en mano de los médicos terapias y tratamientos experimentales contra la covid-19.
Moderna aseguró que espera realizar esta solicitud ante la FDA «en las próximas semanas» y en paralelo iniciar los procesos de autorización con agencias reguladores de otros países y regiones.
Información disponible en:
https://investors.modernatx.com/news-releases/news-release-details/modernas-covid-19-vaccine-candidate-meets-its-primary-efficacy
Conexion Megalabs - Vacuna Moderna
Síndrome de Vexas: enfermedad inflamatoria grave de inicio en el adulto refractaria al tratamiento y a menudo fatal.
Una investigación publicada en el New England Journal of Medicine reveló un nuevo trastorno inflamatorio.
Investigadores del Instituto Nacional de Salud (NIH) de Estados Unidos han descubierto un nuevo trastorno inflamatorio causado por mutaciones en el gen UBA1, cuyos síntomas incluyen coágulos de sangre en las venas, fiebre recurrente, anomalías pulmonares y vacuolas (estructuras inusuales parecidas a cavidades) en las células mieloides.
Utilizando un enfoque impulsado por el genotipo, los autores identifican un trastorno que conecta síndromes inflamatorios de aparición en la edad adulta aparentemente no relacionados. A este trastorno lo llamaron síndrome VEXAS (vacuolas, enzima E1, ligado al cromosoma X, autoinflamatorio, somático).
Los autores encontraron un gen que está muy relacionado con este nuevo síndrome, que puede poner en peligro la vida. Hasta ahora, el 40% de los pacientes con VEXAS que estudió el equipo han muerto, lo que revela las devastadoras consecuencias de la grave afección.
Los autores identificaron a 25 hombres con mutaciones somáticas que afectan a la metionina-41 (p.Met41) en UBA1, la principal enzima E1 que inicia la ubiquitilación (el gen UBA1 se encuentra en el cromosoma X). En estos pacientes se observó un síndrome inflamatorio refractario al tratamiento, a menudo fatal, que se desarrolla al final de la edad adulta caracterizado por fiebre, citopenias, vacuolas características en las células precursoras mieloides y eritroides, médula ósea displásica, neutrófilos cutáneos y neutrofílicos, inflamación pulmonar, condritis y vasculitis. La mayoría de estos 25 pacientes cumplían los criterios clínicos de un síndrome inflamatorio (policondritis recidivante, síndrome de Sweet, poliarteritis nodosa o arteritis de células gigantes) o una afección hematológica (síndrome mielodisplásico o mieloma múltiple) o ambos. Se encontraron mutaciones en más de la mitad de las células madre hematopoyéticas, incluidas las células mieloides de sangre periférica, pero no en los linfocitos ni los fibroblastos. Las mutaciones que presentaban estos pacientes dieron como resultado la pérdida de la isoforma citoplásmica canónica de UBA1 y la expresión de una nueva isoforma catalíticamente alterada. Las células de sangre periférica mutantes mostraron una ubiquitilación disminuida y vías inmunes innatas activadas.
Se espera que este hallazgo ayude a los profesionales de la salud a mejorar las evaluaciones de la enfermedad y proporcione tratamientos apropiados para miles de pacientes que tienen diversas afecciones relacionadas con la inflamación. El estudio también puede allanar el camino para una clasificación nueva y más apropiada de enfermedades inflamatorias.
Artículo disponible en:
https://www.nejm.org/doi/full/10.1056/NEJMoa2026834
Conexion Megalabs -Sindrome de Vexas

La bondad puede darte una sensación de bienestar o tal vez un cálido resplandor a tu día a día
¿Qué significa realmente ser amable y por qué es importante? Daniel Fessler, director del Instituto Bedari Kindness de UCLA afirma que la amabilidad se refiere a «los pensamientos, sentimientos y creencias que, asociadas con acciones, intentan #beneficiar a otros, lo cual es un fin en sí mismo, no un medio para alcanzar un fin».
La falta de amabilidad, por otro lado, consiste en «creencias intolerantes y la falta de valoración del bienestar de los demás». «Vivir con personas que te tratan con desprecio o indiferencia, en el mejor de los casos, y con hostilidad abierta, te hace mal. Acorta tu vida, literalmente», sostiene. «Por el contrario, tanto el recibir amabilidad de los demás como el brindarla, siendo ambas acciones la antítesis de una situación de estrés tóxico, son benéficas».
«Contemplar cómo puedes ser amable con los demás, reduce la presión arterial y tiene beneficios terapéuticos que ayudan a tratar la depresión y la #ansiedad», dice el experto.
Cada persona que conoces está librando una batalla de la que no sabes nada.
¡SÉ AMABLE SIEMPRE!

Ugur Sahin, uno de los científicos detrás de la vacuna de Pfizer, pronosticó cuándo se podrá “volver a la vida normal”
El CEO y cofundador de BioNTech, empresa alemana asociada con Pfizer para el desarrollo de la vacuna contra el coronavirus, adelantó tiempos difíciles incluso cuando se llegue a aplicar la vacuna candidata de Pfizer durante el mes de diciembre.
El científico, que desarrolló en la sede de Mainz, Alemania la vacuna que asegura una eficacia del 90 por ciento, le dijo a Sky News que las personas en el Reino Unido podrían vacunarse contra el coronavirus a partir del próximo mes. El gobierno de Boris Johnson ya está diseñando un operativo para poder cubrir las expectativas de vacunación: hasta los estadios serán utilizados como centros de inyección.
El profesor Sahin puso un único reparo en las fechas: precisó que la inoculación dependería de si el regulador del Reino Unido aprueba la vacuna a tiempo. Según las especulaciones en torno a la publicación de los resultados de Fase 3, el laboratorio estaría pidiendo la autorización de urgencia la próxima semana.
Sahin advirtió que “la aplicación durante la mitad de diciembre no significará que la situación cambiará drásticamente”. “Este será un invierno difícil. Empeorará antes de mejorar”, enfatizó.
Sin embargo, dijo que, con la ayuda de la vacuna, “podríamos volver a la vida normal a mediados del próximo año”.
Luego de los anuncios de Pfizer con respecto al éxito de un 90 por ciento de su candidata, Moscú y su vacuna Sputnik con un 92 por ciento, expertos comenzaron a señalar sus reparos. Muchos científicos manifiestan su consternación por el adelanto de datos y resultados de ensayos clínicos antes de la revisión por pares.
Información disponible en:
https://news.sky.com/story/covid-19-biontech-founder-ugur-sahin-says-first-uk-patients-could-be-vaccinated-next-month-12130523
Conexion Megalabs - Ugur Sahin
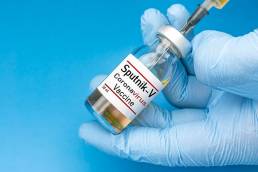
Rusia afirma que su vacuna Sputnik V tiene eficacia de 92%
El primer análisis intermedio de los datos de los ensayos clínicos de fase III en la Federación rusa demostró una eficacia del 92% de la vacuna Sputnik V contra el coronavirus.
La efectividad en la aplicación de la vacuna Sputnik V fue del 92% (el cálculo se basó en la distribución de 20 casos confirmados detectados en el grupo placebo y en el grupo que recibió la vacuna). Actualmente, 40.000 voluntarios están participando en un estudio clínico poscomercialización de fase III, doble ciego, aleatorizado y controlado con placebo de la vacuna Sputnik V, de los cuales más de 20.000 voluntarios han sido vacunados con la primera dosis de la vacuna y más de 16.000 voluntarios con la primera y segunda dosis.
La eficacia se demostró en base al primer análisis de datos provisionales 21 días después de que los voluntarios recibieran su primera inmunización.
Durante las pruebas, no se detectaron efectos adversos inesperados si bien continúa el seguimiento del estado de los participantes.
El primer registro de una vacuna contra la infección por coronavirus en el mundo, llevado a cabo en Rusia el 11 de agosto como parte del procedimiento de examen acelerado de medicamentos, también permite a la Federación Rusa usar la vacuna en voluntarios adicionales fuera de los ensayos clínicos médicos y otros grupos con mayor riesgo de padecer la enfermedad COVID-19. Los ensayos en el marco de la población civil fuera de los ensayos clínicos, basados en la observación de 10.000 personas vacunadas, también mostraron una eficacia de la vacuna superior al 90%.
En la actualidad, también se han aprobado y se están llevando a cabo ensayos clínicos de Fase III en la República de Bielorusia, los Emiratos Árabes Unidos, Venezuela y varios otros países, así como ensayos en Fase II-III en la India.
La vacuna Sputnik V se creó en base a la estudiada y probada plataforma de vectores adenovirales humanos, cuyas importantes ventajas son la seguridad, la eficacia y la ausencia de consecuencias negativas a largo plazo, confirmadas en más de 250 estudios clínicos realizados en el mundo durante dos décadas (la historia del uso de adenovirus humanos en el desarrollo de vacunas comenzó en 1953). Más de 100.000 personas han sido vacunadas con medicamentos aprobados y registrados basados en vectores adenovirales humanos.
La singularidad de la vacuna rusa radica en el uso de dos vectores diferentes basados en el adenovirus humano, lo que permite una respuesta inmune más potente y duradera como resultado de la segunda inmunización.
Información completa disponible en:
https://sputnikvaccine.com/esp/newsroom/pressreleases/el-primer-an-lisis-intermedio-de-los-datos-de-los-ensayos-cl-nicos-de-fase-iii-en-la-federaci-n-rusa/
Conexion Megalabs - Vacuna Sputnik V tiene eficacia de 92%