En medio de un número creciente de casos en un país tras otro, Europa estaría al borde de una segunda ola de COVID-19
Mientras que países como España, Francia y Alemania fueron testigos ayer de los mayores incrementos diarios en meses, funcionarios y expertos están discutiendo si la segunda ola está aquí o no.
España registró saltos significativos tanto en hospitalizaciones como en nuevas infecciones en las últimas semanas.
A pesar de estar presenciando la aceleración más rápida del contagiode COVID-19 en Europa, los expertos en España están divididos sobre si llamarlo o no una segunda ola.
El 23 de julio, cuando el epidemiólogo jefe de España, Fernando Simon, estaba de vacaciones y los casos comenzaron a aumentar, su sustituto, la Dra. María José Sierra, dijo: «Es posible que estemos en una segunda ola».
La viróloga Margarita del Val estaba aún más segura. “Creo que estamos en una segunda ola. Será más pequeña que la primera, pero espero que reaccionemos. Aunque lo malo es que se transmite en silencio, por lo que en cualquier momento podría aparecer y asustarnos «, dijo a los medios a fines de julio.
Sin embargo, a su regreso, Fernando Simon era mucho más escéptico. Hace apenas una semana, mientras los casos seguían aumentando, dijo que si España estaba en una segunda ola «ciertamente no lo parece … la gente puede llamarlo como quieran, pero lo que estamos detectando ahora son brotes y un cierto grado de transmisión comunitaria en ciertos lugares «.
El gobierno español también ha evitado usar el término. En cambio, los esfuerzos se han centrado en calificar al país como un destino turístico «seguro» a la luz de varios países europeos que imponen cuarentena a las llegadas desde España. Es un tema de definición política, pero la cantidad de nuevos casos diarios en España es claramente objetivable.
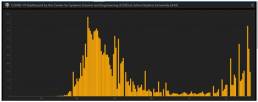
Incremento de casos en España
Francia: mayor aumento diario en meses
Los nuevos casos en Francia se han reportado en su punto más alto desde el 30 de mayo, según las últimas cifras del Ministerio de Salud y la Dirección General de Salud.
Hay un mayor número de infecciones diarias por coronavirus en las últimas 24 horas: 1,695 contagios más.
Desde el comienzo de la pandemia, el número total de infecciones en Francia es de 194,029 y el número de muertes de 30,305.
El número de hospitalizaciones ha disminuido, junto con el de los casos de cuidados intensivos. Unas 5.148 personas permanecen hospitalizadas con 384 en cuidados intensivos. Actualmente, 14 departamentos dentro de Francia se consideran dentro de una situación vulnerable. Hay 187 grupos colectivos de infección que permanecen bajo investigación en el país, un aumento de 16 en las últimas 24 horas.
Italia cautelosa tras aumento de nuevos casos
El número de nuevos casos confirmados de COVID-19 en Italia se duplicó a 384 el miércoles, mientras que el país registró 10 nuevas muertes. Eso lleva el número total de casos en Italia a 248,803 y el número de muertos a 35,181, según los últimos datos del Ministerio de Salud. Las infecciones activas se sitúan en 12.646. A pesar del salto del miércoles en nuevas infecciones, el número de casos diarios en Italia ha oscilado entre 200 y 300 durante semanas.
Han surgido algunos grupos pequeños en las regiones italianas, pero están relacionados principalmente con personas que llegan del extranjero. Los científicos y las autoridades creen que Italia ha logrado evitar una segunda ola de contagios, pero siguen advirtiendo a los italianos, que están entrando en la cima de la temporada de vacaciones, que no bajen la guardia.
La próxima gran prueba, según los expertos, será la reapertura de las escuelas en septiembre.
Alemania registra un fuerte aumento
A pesar de su éxito en la lucha contra la pandemia de coronavirus a principios de este año, Alemania también fue testigo de un fuerte aumento en los casos de coronavirus esta semana. El jueves, la agencia alemana de control y prevención de enfermedades Robert Koch Institute (RKI) informó el mayor número de casos diarios nuevos en tres meses.
Según RKI, 1,045 personas dieron positivo por coronavirus en el país en las últimas 24 horas, y por primera vez el número superó las 1,000 desde mayo. Esto ocurrió solo dos días después de que Marburger Bund, un sindicato nacional que representa a los médicos, advirtió que el país ya estaba experimentando una segunda ola del virus. Los médicos advirtieron que la segunda ola puede golpear más fuerte ya que las personas dejaron de obedecer las medidas de distanciamiento social debido a su anhelo de volver a la normalidad.
Los números diarios aumentan desde julio en Bélgica
La semana pasada se registró un promedio diario de 531 nuevas infecciones por coronavirus en Bélgica, confirmó el jueves el Instituto de Salud Pública del país, Sciensano. El miércoles, 510 personas más fueron diagnosticadas con COVID-19.
El número de infecciones ha aumentado continuamente desde principios de julio. Entre el 20 de julio y el 2 de agosto, se registraron un promedio de 54 nuevos casos diarios por cada 100,000 habitantes, que es 198% más que las dos primeras semanas del mes. También hubo un ligero aumento en el número de muertes durante el período comprendido entre el 27 de julio y el 2 de agosto. En promedio, tres personas perdieron la vida debido a COVID-19, un crecimiento del 30% en comparación con la semana anterior.
En total, 71.158 personas han sido infectadas con el nuevo coronavirus desde el inicio del brote y 9.852 personas perdieron la vida. Mientras tanto, los principales expertos belgas en virus debaten si la segunda ola de la pandemia ya ha llegado.
El Dr. Steven Van Gucht, jefe de enfermedades virales de Scieansano, a principios de esta semana en una conferencia de prensa dijo: «Estamos en la segunda ola de infecciones, y nadie sabe cuánto tiempo llevará o qué tan intenso será».
Pero según Frederique Jacobs, el portavoz del gobierno inter-federal a cargo de combatir el coronavirus, aún no es la segunda ola, sino «solo un aumento de las infecciones que podrían conducir a la segunda ola».
En una entrevista con la televisión RTL, recordó que «durante el pico de la crisis del coronavirus, se diagnosticaron entre 2.000 y 2.500 nuevas infecciones cada día».
Expertos advierten al gobierno británico de la segunda ola
Investigadores británicos también advirtieron al gobierno el martes que la reapertura de las escuelas en septiembre sin implementar primero un sistema eficaz de prueba, rastreo y aislamiento podría dar como resultado una segunda ola de COVID-19 que podría ser el doble de fuerte que la primera. El gobierno también ordenó a las compañías farmacéuticas que acumulen medicamentos para compensar los riesgos de un Brexit sin acuerdo.
En el mejor de los casos con un sistema de prueba, rastreo y aislamiento efectivo, «se podría prevenir un rebote epidémico», pero en el peor de los casos, la segunda ola podría ser 2.3 veces mayor que la primera.
El Reino Unido reportó 892 casos nuevos el miércoles, mientras que reportó 670 un día antes.
Desde su aparición en China en diciembre pasado, el virus se ha extendido a al menos 188 países y regiones, según las cifras compiladas por el Centro de Recursos de Coronavirus de la Universidad Johns Hopkins, con sede en Estados Unidos.
Se han confirmado más de 19 millones de casos de COVID-19 en todo el mundo, con muertes superiores a 708,000 y más de 11.3 millones recuperados
Europa estaría al borde de una segunda ola de COVID-19

Johnson & Johnson firma acuerdo de mil millones de dólares para suministrar a los EE. UU. la vacuna COVID-19
Ref: PR Newswire, CNBC, Bloomberg, NASDAQ, Yahoo News, London South East, Morningstar, HHS, MarketWatch, TheStreet
PUBLICADO: 5 DE AGOSTO DE 2020
Anna Bratulic
Johnson & Johnson dijo el miércoles que firmó un acuerdo con el gobierno de EE. UU. para la fabricación nacional a gran escala y la entrega de 100 millones de dosis de su vacuna experimental SARS-CoV-2 Ad26.COV2.S para su uso en el país.
Específicamente, la Autoridad de Investigación y Desarrollo Biomédico Avanzado de EE. UU. (BARDA) ha comprometido más de US$1000 millones en virtud de este acuerdo de fabricación de vacunas, mientras que el gobierno también tiene la opción de adquirir dosis adicionales de Ad26.COV2. Se dice que sería suficiente para vacunar a 300 millones de personas.
Paul Stoffels, director científico de Johnson & Johnson, declaró que «apreciamos enormemente la confianza y el apoyo del gobierno de EE. UU en nuestra plataforma y esfuerzos de I + D y la escalabilidad de nuestra tecnología de vacunas». La compañía está apuntando a más de mil millones de dosis en todo el mundo a lo largo de 2021, y Stoffels señaló que «estamos ampliando la producción en los Estados Unidos y en todo el mundo para entregar una vacuna SARS-CoV-2 para uso de emergencia».
Según el Departamento de Salud y Servicios Humanos de los EE. UU. (HHS), BARDA ha proporcionado hasta ahora aproximadamente US$ 456 millones para ensayos clínicos y otras actividades de desarrollo de vacunas bajo una asociación a largo plazo existente con Johnson & Johnson.
Pruebas clínicas en curso.
La compañía inició recientemente un ensayo de fase I / II de Ad26.COV2.S en voluntarios sanos en los EE. UU. Y Bélgica. Ese estudio, junto con un posible ensayo de Fase III que podría comenzar en septiembre, probará paralelamente los regímenes de una y dos dosis de la vacuna basada en el vector de adenovirus serotipo 26 (Ad26).
El HHS señaló que si se usa en el curso de una campaña de vacunación contra COVID-19, Ad26.COV2.S se pondría a disposición del pueblo estadounidense sin costo alguno, aunque los profesionales de la salud podrían cobrar por administrar la vacuna. El departamento de salud también dijo que el último acuerdo incluye la fabricación, llenado y acabado en instalaciones con sede en los EE. UU., un paso que asegura que garantizará que las dosis de la vacuna estén listas para enviarse de inmediato, en espera de ensayos clínicos exitosos y la autorización de la FDA.
El acuerdo de Estados Unidos es el primer acuerdo de Johnson & Johnson para suministrar su vacuna en investigación a un país. Mientras tanto, la compañía está en conversaciones con la UE, pero aún no se ha alcanzado un acuerdo.
Johnson & Johnson firma acuerdo de mil millones de dólares

América Latina: la región más afectada por COVID19
El martes, América Latina superó a Europa para convertirse en la región con el mayor número de muertes reportadas por SARSCoV2. Con más de 210,000 muertes, la región representa aproximadamente el 30% de las muertes totales por COVID19 reportadas en el mundo.
El virus tardó más en afectar a América Latina que otras regiones, pero países como Colombia, Perú, Argentina y Bolivia ahora están experimentando un fuerte aumento en el número de casos de COVID-19. Una interpretación más realista de este fenómeno debe incluir el tiempo requerido para el desarrollo de la capacidad diagnóstica en cada territorio: la propagación de la pandemia se ha acelerado en esos países junto con el desarrollo de la capacidad diagnóstica.
Brasil, el país latinoamericano más afectado por el nuevo coronavirus, ha registrado un total de 95,819 muertes hasta el martes. México, el segundo país más afectado en la región, ha informado 48,869 muertes.
La semana pasada, América Latina se convirtió en la región más afectada del mundo, considerando el número de casos. Hoy miércoles 5 de agosto el número de infecciones reportadas superó los 5.3 millones, según recuentos basados en datos de los gobiernos y recogidos por el Centro de Ingenieria de la Universidad Johns Hopkins
El número de casos aumentó después de que las autoridades de varios países, particularmente Brasil, relajaron las medidas de cierre para estimular la actividad económico y al mismo tiempo incrementaron la capacidad diagnóstica.
El virus ha infectado a más de 18.4 millones de personas en todo el mundo. La cifra global de muertes (reportadas) es superior a 702.000.
Conviviendo con SARSCoV2
Italia, Alemania, España y otros países europeos se preparan para un segundo pico de casos entre setiembre y octubre, al tiempo que se acelera el reporte de casos nuevos desde India, Sureste Asiático, Africa y Australia, coincidiendo con la relajación de las medidas de distanciamiento social y con el despliegue de mayor capacidad diagnóstica. Teniendo en cuenta la alta transmisibilidad del virus, el crecimiento exponencial del número de casos, la ausencia de estacionalidad del CoV2 (se transmite tanto en verano como en invierno) y la imposibilidad de mantener el confinamiento en forma indefinida, hacia fin de año puede proyectarse un número de casos y de muertes superior al doble de los informados hoy.
La introducción de una vacuna eficaz con campañas intensas de vacunación masiva en Estados Unidos y en Europa durante el invierno boreal, no lograría detener la transmisión ni el aumento de casos hasta marzo-abril del año próximo, considerando el tiempo que se ha informado para el desarrollo de inmunidad.
La extensión de la vacunación hacia el resto del mundo y la duración de la inmunidad adquirida no pueden predecirse en este momento, de manera que la única seguridad que tenemos es la persistencia del virus en el ecosistema humano durante un período indefinido de años. Un virus capaz de subsistir durante semanas en portadores humanos asintomáticos, superficies metálicas inertes e incluso en animales como el perro.
Ante la imposibilidad de detener la economía y el avance material durante períodos de tiempo indefinidos, la única alternativa es aprender a convivir con el coronavirus y con las consecuencias de la enfermedad.
América Latina la región más afectada por COVID19

Existen Diferencias en los niveles de SARS-CoV-2 relacionados con la edad, en pacientes con enfermedad por coronavirus (COVID-19) leve a moderada.
Los niños son susceptibles a la infección por SARS-CoV-2 responsable del síndrome respiratorio agudo severo (SARS-CoV-2), pero generalmente presentan síntomas leves en comparación con los adultos.
Los niños en muchas ocasiones transmiten ciertas enfermedades respiratorias y gastrointestinales en la población, pero los datos existentes sobre niños como fuente de transmisión de SARS-CoV-2 son escasos.
Los primeros informes no encontraron evidencia sólida de niños como principales causantes de la propagación del SARS-CoV-2, pero el cierre de las escuelas al comienzo de la pandemia frustró las investigaciones a gran escala de las escuelas como fuente de transmisión comunitaria. A medida que los sistemas de salud pública buscan reabrir las escuelas y retomar el día a día, importa comprender la potencial de transmisión de niños y así orientar las medidas de salud pública.
En este artículo se informa que la replicación del SARS-CoV-2 en niños mayores presenta niveles similares a la de los adultos, pero se detectan significativamente mayores cantidades de ácido nucleico viral en niños menores de 5 años.
En el presente trabajo realizado entre el 23 de marzo y el 27 de abril de 2020, se analizaron varios hisopados nasofaríngeos mediante la reacción en cadena de la polimerasa (PCR) para detección SARS-CoV-2. Los hisopados fueron recogidos durante hospitalización, consulta externa, departamento de emergencias y sitios de pruebas de manejo en un centro médico terciario pediátrico en Chicago, Illinois.
Se registraron los valores del umbral del ciclo de amplificación por PCR (CT), con valores más bajos que indicaban mayor cantidad de ácido nucleico viral.
La cohorte incluyó pacientes de 1 mes a 65 años que dieron positivo para SARS-CoV-2. Se evaluaron pacientes con síntomas sugestivos de enfermedad compatible con COVID-19 y / o aquellos con exposiciones de alto riesgo.
Debido a que los pacientes con infección grave tienen valores de CT más bajos, se excluyeron a 7 niños que requirieron apoyo con oxígeno suplementario. También se excluyeron a 7 pacientes asintomáticos, 29 pacientes con duración desconocida de los síntomas, y 19 pacientes cuyos síntomas comenzaron más de 1 semana antes de la prueba.
Los hisopados se recolectaron utilizando un procedimiento de muestreo nasofaríngeo bilateral estándar.
Los autores informan que la cohorte final incluyó 145 pacientes con enfermedad leve a moderada con 1 semana desde el inicio de los síntomas. Compararon 3 grupos: niños pequeños menores de 5 años (n = 46), niños mayores de 5 a 17 años (n = 51) y adultos de 18 a 65 años (n = 48). Encontraron una media similar de CT para niños mayores (11.1 [6.3-15.7]) y adultos (11.0 [6.9- 17.5]). Sin embargo, los niños pequeños tuvieron valores de CT significativamente más bajos (6.5 [4.8-12.0]), lo que indica que los niños pequeños tienen una cantidad equivalente o mayor de ácido nucleico viral en el tracto respiratorio superior en comparación con niños mayores y adultos. Las diferencias observadas en la mediana y los valores de CT entre niños pequeños y adultos se aproximan a una cantidad de SARS-CoV-2 de 10 a 100 veces mayor en el tracto respiratorio superior de niños pequeños.
El análisis sugiere que niños menores de 5 años con COVID-19 leve a moderado tienen altas cantidades de ARN viral de SARSCoV-2 en su nasofaringe en comparación con niños mayores y adultos. Si bien el estudio se limita a la detección de ácido nucleico viral, en lugar de virus, son varios los estudios pediátricos de SARSCoV-2 que informaron una correlación entre un mayor nivel de ácido nucleico y la capacidad de cultivar virus.
Los autores concluyen que los niños pequeños pueden ser potencialmente importantes en la transmisión de SARS-CoV-2 a la población general, como se ha demostrado con el virus sincicial respiratorio, en el cual es más probable que los niños transmitan altas cargas virales. Los hábitos de comportamiento de niños pequeños, las escuela y guarderías plantean preocupación por la posible amplificación de la infección por SARS-CoV-2 en esta población a medida que se disminuyen las restricciones de salud pública y se reinicia la actividad escolar.
Niños y COVID

Compromiso del sistema nervioso después de la infección con COVID-19 y otros coronavirus
Resumen
Las infecciones virales tienen efectos perjudiciales en las funciones neurológicas, e incluso pueden causar daños neurológicos graves. Muy recientemente, los coronavirus (CoV), especialmente el del síndrome respiratorio agudo severo CoV 2 (SARS-CoV-2), exhibe propiedades neurotrópicas y también pueden causar enfermedades neurológicas. Se informa que el CoV se puede encontrar en el cerebro o en el líquido cefalorraquídeo. La biopatología de estos virus neuroinvasivos aún no se conoce de manera completa y, por lo tanto, es importante explorar el impacto de las infecciones por CoV en el sistema nervioso. Aquí, revisamos la investigación sobre las complicaciones neurológicas en las infecciones por CoV y los posibles mecanismos de daño al sistema nervioso.
1. Introducción
En diciembre de 2019, la epidemia de la Enfermedad del Virus Corona 2019 (COVID-19) surgió en Wuhan, China. El virus se conoce como coronavirus 2 del síndrome respiratorio agudo especialmente severo (SARS-CoV-2). Recientemente se documentó que, además de los síntomas sistémicos y respiratorios, el 36.4% (78/214) de los pacientes con COVID-19 desarrollan síntomas neurológicos, como dolor de cabeza, alteración de la conciencia y parestesia. Los pacientes gravemente afectados tienen más probabilidades de desarrollar síntomas neurológicos que los pacientes con enfermedad leve o moderada. Además, los informes de autopsias han revelado edema de tejido cerebral y degeneración neuronal parcial en pacientes fallecidos.
El 4 de marzo de 2020, el Hospital Ditan de Beijing informó por primera vez un caso de encefalitis viral causada por un nuevo coronavirus (CoV) que ataca al sistema nervioso central (SNC). Los investigadores confirmaron la presencia de SARS-CoV-2 en el líquido cefalorraquídeo por secuenciación del genoma. Esto hace pensar que COVID-19 tiene el potencial de causar daño al sistema nervioso. Con la actual pandemia de COVID-19, es particularmente necesario informar a los médicos sobre el impacto de varias infecciones por CoV en el SNC. Este artículo revisa la epidemiología, los posibles mecanismos de neuroinvasión y las estrategias de manejo relacionadas con las infecciones por CoV con posible afectación del sistema nervioso.
2. Infecciones por CoV que afectan el SNC
Muchas infecciones virales pueden causar daños graves a la estructura y función del sistema nervioso, incluida la encefalitis grave debida a infecciones virales en el SNC, encefalopatía tóxica causada por infecciones virales sistémicas graves y lesiones desmielinizantes agudas graves que se desarrollan después de infecciones virales. Algunos virus son neurotrópicos y pueden invadir los tejidos nerviosos y causar infecciones de macrófagos, microglia o astrocitos que funcionan inmunológicamente en el SNC.
Los CoV tienen un diámetro promedio de 100 nm y son esféricos u ovalados. Hay grandes picos de glicoproteínas de membrana viral en la superficie y, cuando se observan por microscopía electrónica, estas partículas de virus teñidas negativamente muestran una forma típica de corona. El CoV es un virus de ARN monocatenario de sentido positivo, que alberga el genoma más grande entre los virus de ARN conocidos actualmente, con una longitud del genoma de aproximadamente 26–32 kb. El agente patógeno del nuevo brote de neumonía en curso es el nuevo CoV 2019 (SARS-CoV-2), que es el séptimo CoV conocido que puede infectar a los humanos; los seis restantes son HCoV-229E, HCoV-OC43, HCoV-NL63, HCoV-HKU1, SARS-CoV y MERS-CoV. Los tipos más comunes e importantes de infecciones por CoV con daño potencial al sistema nervioso se describen a continuación.
2.1. SARS-CoV
El síndrome respiratorio agudo severo (SARS) es una enfermedad respiratoria zoonótica causada por el SARS-CoV que comenzó en Asia y se extendió por todo el mundo en 2003. Tiene las características de inicio agudo y una fuerte infectividad, y es una gran amenaza para la salud humana. Las principales manifestaciones clínicas del SARS son fiebre, escalofríos, tos seca y dificultad para respirar. En casos severos, puede ocurrir insuficiencia respiratoria y muerte. Además, el SARS-CoV podría inducir enfermedades neurológicas como la polineuropatía, la encefalitis y el accidente cerebrovascular isquémico aórtico. Los estudios de autopsia demostraron que podían detectarse signos de edema cerebral y vasodilatación meníngea en la mayoría de los casos de SARS. Además, podría detectarse en el cerebro la infiltración de monocitos y linfocitos en la pared de los vasos, cambios isquémicos de las neuronas, desmielinización de las fibras nerviosas, así como las partículas del virus SARS-CoV y las secuencias del genoma.
2.2. MERS-CoV
El Síndrome Respiratorio del Medio Oriente (MERS), causado por MERS-CoV, se origina en los murciélagos, y el huésped intermedio es el camello. Los pacientes con infección por MERS-CoV generalmente presentan síntomas relacionados con la neumonía, como fiebre, mialgia, tos y disnea. Los casos graves pueden conducir al síndrome de dificultad respiratoria aguda (SDRA), shock séptico, insuficiencia orgánica múltiple y muerte. Se sabe que MERS-CoV es potencialmente neuroinvasivo, y que un estudio retrospectivo encontró que el 25.7% de los pacientes con MERS pueden desarrollar síntomas neuropsiqiuiatricos y el 8.6% de los pacientes tienen convulsiones. También se informó que casi 1/5 de los pacientes con infección por MERS-CoV muestran síntomas neurológicos durante el proceso de infección, incluidos, entre otros, trastornos de la conciencia, parálisis, accidente cerebrovascular isquémico, síndrome de Guillain-Barré y otras intoxicaciones o neuropatía infecciosa. Curiosamente, sus complicaciones neurológicas no se acompañan de síntomas respiratorios, sino que se retrasan de 2 a 3 semanas.
2.3. SARS-CoV-2
La similitud genética entre SARS-CoV-2 y SARS-CoV es de 79.5%, y su similitud con el coronavirus de murciélago es de 96%. Los pacientes infectados con SARS-CoV-2 tienen síntomas de diversos grados, que van desde fiebre o tos leve hasta neumonía y una amplia participación de múltiples funciones orgánicas con una tasa de mortalidad del 2% al 4%. En la actualidad, los datos clínicos han revelado que algunos pacientes con COVID-19 tienen síntomas similares a las infecciones intracraneales, como dolor de cabeza, epilepsia y alteración de la conciencia. Además, un número creciente de pacientes con COVID-19 informan una pérdida repentina del olfato o del sabor. Por lo tanto, es probable que se observe anosmia y disgeusia en pacientes con COVID-19. De hecho, algunos pacientes incluso desarrollan síntomas relacionados con COVID-19 solo después de mostrar síntomas neurológicos. Recientemente, el Hospital Ditan de Beijing reportó por primera vez un caso de encefalitis viral causada por el nuevo CoV que ataca el SNC. Los investigadores confirmaron la presencia de SARS-CoV-2 en el líquido cefalorraquídeo mediante secuenciación del genoma, agregando apoyo a la teoría de que este nuevo virus de la neumonía también puede causar daño al sistema nervioso. Por lo tanto, es probable que otros patógenos, como las bacterias, puedan destruir la barrera hematoencefálica, y las infecciones intracraneales secundarias pueden causar dolores de cabeza, vómitos en chorro, pérdida visual y convulsiones de extremidades en pacientes con síntomas graves de COVID-19.
3. Enfermedades del sistema nervioso relacionadas con infecciones por CoV
3.1 Encefalitis viral
La encefalitis se refiere a lesiones inflamatorias en el parénquima cerebral causadas por agentes patógenos, incluido el daño neuronal y las lesiones del tejido nervioso. Se caracteriza por un inicio agudo, y los síntomas comunes incluyen dolor de cabeza, fiebre (principalmente fiebre alta), vómitos, convulsiones y trastornos de la conciencia. El diagnóstico precoz de la encefalitis viral es crítico. En la epidemia de neumonía en curso, el equipo de tratamiento del Hospital Ditan de Beijing confirmó la presencia de SARS-CoV-2 en el líquido cefalorraquídeo de pacientes con COVID-19 por secuenciación del genoma, verificando clínicamente la encefalitis viral. Esto proporcionó una base sólida para el CoV que causa la encefalitis.
3.2. Encefalopatía tóxica infecciosa
La encefalopatía tóxica infecciosa, también conocida como encefalitis tóxica aguda, se refiere a un tipo de síndrome de disfunción cerebral reversible causado por factores como toxemia sistémica, trastornos metabólicos e hipoxia durante el proceso de infección aguda. Los cambios patológicos básicos en esta enfermedad incluyen edema cerebral, sin evidencia de inflamación en el análisis del líquido cefalorraquídeo. Sus síntomas clínicos son complejos y diversos. Los pacientes con un curso leve de la enfermedad pueden desarrollar dolor de cabeza, disforia, trastorno mental y delirio. Los pacientes gravemente afectados pueden experimentar desorientación, pérdida de conciencia, coma y parálisis. La infección viral aguda también es una causa importante de esta enfermedad, ejemplificada por una infección respiratoria causada por CoV. Los pacientes con COVID-19 a menudo sufren de hipoxia severa y viremia, que tiene el potencial de causar encefalopatía tóxica. Además, casi el 40% de los pacientes con COVID-19 desarrollan dolor de cabeza, alteración de la conciencia y otros síntomas de disfunción cerebral, y un estudio de autopsia informó que se ha detectado edema en el tejido cerebral de pacientes con COVID-19. En conjunto, estos hallazgos proporcionan la evidencia de que COVID-19 podría causar encefalopatía tóxica infecciosa, aunque se requieren estudios detallados.
3.3. Enfermedad cerebrovascular aguda
Una cantidad considerable de evidencia indica que la infección relacionada especialmente con las vías respiratorias es un factor de riesgo independiente para la enfermedad cerebrovascular aguda. Los datos del uso de modelos experimentales de ratones sugieren que el virus de la influenza puede agravar la lesión cerebral isquémica al desencadenar una cascada de citocinas y aumentar el riesgo de hemorragia cerebral después del tratamiento con activador de plasminógeno de tipo tisular. Se ha informado ampliamente que la infección de CoV, especialmente el SARS-CoV-2, causa síndrome de tormenta de citoquinas, que pueden ser uno de los factores que causan la enfermedad cerebrobasilar aguda. Además, los pacientes críticos con infecciones graves por SARS-CoV-2 a menudo muestran niveles elevados de dímero D y reducción plaquetaria severa, lo que puede hacer que estos pacientes sean propensos a eventos cerebrovasculares agudos. Por lo tanto, es probable que durante las infecciones por CoV, los pacientes en riesgo de desarrollar enfermedad cerebrovascular sean alertados con respecto a la ocurrencia de eventos cerebrovasculares agudos.
4. Mecanismos de las infecciones por CoV sobre el daño del sistema nervioso.
4.1. Lesión por infección directa
El material genético e incluso las proteínas de varios virus a menudo se pueden detectar en muestras de tejido del sistema nervioso (como el líquido cefalorraquídeo o el cerebro), lo que sugiere que los virus pueden invadir directamente el sistema nervioso y causar daño neurológico.
4.1.1 Vía de circulación de la sangre
Un virus típico que ingresa al SNC a través de la circulación sanguínea es el virus JE, que se multiplica en las células vasculares del área de la piel afectada por la picadura del mosquito. Posteriormente se libera en la sangre para reproducirse en macrófagos mononucleares en todo el organismo. La liberación secundaria a la sangre puede aumentar la permeabilidad de la barrera hematoencefálica a través de las citocinas producidas, promoviendo así que el virus ingrese al cerebro y causando encefalitis viral. Aunque existen pruebas poco frecuentes de que el CoV, especialmente el SARS-CoV-2, invada el sistema nervioso a través de la vía de circulación sanguínea, se esperan estudios posteriores.
4.1.2. Vía neuronal
La vía neuronal es un vehículo importante para que los virus neurotrópicos ingresen al SNC. Los virus pueden migrar infectando las terminaciones nerviosas sensoriales o motoras, logrando el transporte neuronal retrógrado o anterógrado a través de las proteínas motoras, la dineína y las kinesinas. Un ejemplo de una vía neuronal es la del transporte neuronal olfatorio. La organización anatómica única de los nervios olfativos y el bulbo olfatorio en la cavidad nasal y el prosencéfalo lo convierten efectivamente en un canal entre el epitelio nasal y el SNC.
Como consecuencia, el CoV puede ingresar al cerebro a través del tracto olfativo en las primeras etapas de infección nasal. Por ejemplo, después de que el CoV infecta las células nasales, puede alcanzar todo el cerebro y el líquido cefalorraquídeo a través del nervio olfativo y el bulbo olfatorio en 7 días y causar inflamación y reacción desmielinizante. Sin embargo, la eliminación del bulbo olfativo en los ratones resultó en una invasión restringida de CoV en el SNC. Gu y col. también detectaron partículas del virus del SARS y secuencias del genoma en neuronas cerebrales. Las observaciones mencionadas aquí indican que CoV puede invadir el SNC desde la periferia a través de las vías neuronales.
4.2. Lesión por hipoxia
Cuando el virus prolifera en las células del tejido pulmonar, causa exudación inflamatoria alveolar e intersticial difusa, edema y la formación de membranas transparentes. Esto, a su vez, conduce a trastornos del intercambio de gases alveolares que causan hipoxia en el SNC, aumentando el metabolismo anaeróbico en las mitocondrias de las células cerebrales. La acumulación de ácido puede causar vasodilatación cerebral, inflamación de las células cerebrales, edema intersticial, obstrucción del flujo sanguíneo cerebral e incluso dolor de cabeza debido a isquemia y congestión. Si la hipoxia continúa sin cesar, el edema cerebral y el trastorno de la circulación cerebral pueden empeorar bruscamente. Con la hipertensión intracraneal, la función cerebral se deteriora gradualmente y se puede observar somnolencia, edema conjuntival bulbar e incluso coma. Además, para pacientes con un riesgo particular de desarrollar enfermedad cerebrovascular, la hipoxia también puede inducir la aparición de enfermedad cerebrovascular aguda, como accidente cerebrovascular isquémico agudo. Debido al hecho de que los pacientes con COVID-19 a menudo sufren de hipoxia severa, la lesión por hipoxia puede causar daños posteriores en el sistema nervioso
4.3. Lesión inmune
El daño del sistema nervioso causado por la infección viral puede estar mediado por el sistema inmune. La patología de las infecciones virales graves está estrechamente relacionada con el desarrollo de un síndrome de respuesta inflamatoria sistémica (SIRS). El SIRS podría iniciarse de manera anormal en la neumonía severa causada por la infección por CoV, mientras que la intervención antiinflamatoria temprana previene eficazmente el daño inmune y reduce el riesgo de lesiones en el sistema nervioso. Además, el SARS y COVID-19 han provocado una gran cantidad de muertes, la mayoría de las cuales se han debido a fallas en múltiples órganos (MOF) causadas por SIRS inducidos por virus o trastornos inmunes similares a SIRS. La persistencia de las infecciones por CoV y su capacidad para infectar macrófagos, microglia y astrocitos en el SNC son particularmente importantes. Un virus neurotrópico puede activar las células gliales e inducir un estado proinflamatorio. La interleucina (IL) -6, un miembro importante de la tormenta de citoquinas, se correlaciona positivamente con la gravedad de los síntomas de COVID-2019. Además, los experimentos han confirmado que las células gliales primarias cultivadas in vitro secretan una gran cantidad de factores inflamatorios como IL-6, IL-12, IL-15 y TNF-α después de ser infectados con CoV. Además, la activación de las células inmunes en el cerebro causará inflamación crónica y daño cerebral.
4.4. Enzima convertidora de angiotensina 2
La enzima convertidora de angiotensina 2 (ACE2) es un factor de protección vascular cardio-cerebral que existe en una variedad de órganos, incluidos el sistema nervioso y los músculos esqueléticos, y desempeña un papel importante en la regulación de la presión arterial y los mecanismos de lucha contra la aterosclerosis. Mientras tanto, ACE2 también es un objetivo importante para varios CoV y virus de la influenza. Al unirse a los receptores ACE2, los virus mencionados anteriormente pueden causar presión arterial anormalmente elevada y aumentar el riesgo de hemorragia cerebral. Además, dado que la proteína espiga de SARS-CoV-2 podría interactuar con ACE2 expresada en el endotelio capilar, el virus también puede dañar la barrera hematoencefálica e ingresar al SNC al atacar el sistema vascular.
4.5. Otros
Las propiedades biológicas del SNC pueden facilitar la exacerbación del daño neurológico causado por las infecciones por CoV. El SNC tiene una estructura parenquimatosa densa y la falta habitual de permeabilidad de sus vasos sanguíneos es una barrera para la invasión de virus. Sin embargo, si un virus obtiene acceso al SNC, es difícil eliminarlo. Debido a la falta de antígenos complejos de histocompatibilidad importantes en las células nerviosas, la eliminación de virus en las células nerviosas depende únicamente del papel de las células T citotóxicas; Sin embargo, la apoptosis de las neuronas maduras después de la infección por el virus también tiene un efecto relativamente protector. Además, las características de la homeostasis de las células en el SNC también contribuyen a la existencia continua del virus.
5. Conclusión
Las infecciones por CoV pueden afectar el sistema nervioso, y actualmente se cree que el CoV junto con los mecanismos inmunes del huésped puede convertir estas infecciones en afecciones persistentes que pueden conducir a enfermedades neurológicas. Por lo tanto, los pacientes con infección por CoV deben ser evaluados temprano para detectar síntomas neurológicos, como dolor de cabeza, trastorno de la conciencia, parestesia y otros signos patológicos. El análisis oportuno del líquido cefalorraquídeo y el conocimiento y manejo de las complicaciones neurológicas relacionadas con la infección son claves para mejorar el pronóstico de los pacientes críticos.
Compromiso del sistema nervioso

Un estudio halla que los sobrevivientes de COVID-19 muestran una mayor tasa de trastornos psiquiátricos
Un estudio publicado en la revista Brain, Behavior and Immunity (1) el 30 de Julio del 2020 y publicado por expertos del hospital San Raffaele de Milán, halló que más de la mitad de las personas que recibieron tratamiento hospitalario por COVID-19 comenzaron a padecer un trastorno psiquiátrico un mes después de ser tratados por el virus.
De los 402 pacientes sobrevivientes a COVID-19 (265 hombres y 137 mujeres) monitoreados un mes después del tratamiento hospitalario, se encontró que el 56% tenía al menos un trastorno psiquiátrico. Los resultados, basados en entrevistas clínicas y cuestionarios de autoevaluación, mostraron trastorno de estrés postraumático (TEPT) en el 28% de los casos, depresión en el 31% y ansiedad en el 42%. Además, el 40% de los pacientes tenía insomnio y el 20% tenía síntomas obsesivo-compulsivos (OC).
El estudio encontró que las mujeres, que tienen menor probabilidad de muerte por COVID-19 que los hombres, presentaron mayor incidencia de depresión y ansiedad. Los pacientes con diagnósticos psiquiátricos previos positivos mostraron mayores puntajes en las medidas psicopatológicas. Adicionalmente, el índice de inflamación inmunológica sistémica basal (SII, systemic immuneinflammation index), que refleja la respuesta inmune y la inflamación sistémica en función de recuento de linfocitos periféricos, neutrófilos y plaquetas, estuvo asociado positivamente con puntuaciones de depresión y ansiedad.
Los autores afirman que los efectos psiquiátricos podrían ser causados por la respuesta inmune al virus en sí, o por factores estresantes psicológicos como el aislamiento social, el impacto psicológico de una nueva enfermedad grave y potencialmente mortal, las preocupaciones sobre infectar a otros y el estigma. La respuesta inmune a los coronavirus induce la producción local y sistémica de citocinas, quimiocinas y otros mediadores inflamatorios. Pacientes con COVID-19, SARS y MERS muestran altos niveles de interleucina (IL) -1β, IL-6, interferón (IFN) -γ, CXCL10 y CCL2, sugiriendo una activación de la función de la célula T-helper-1. Además, particularmente en COVID-19 (a diferencia del SARS y MERS), se encontraron niveles elevados de citocinas secretadas por células T-helper-2 (como IL-4 e IL-10). Las concentraciones más altas de estas citocinas parecen sugerir una evolución clínica más severa. La desregulación de las citocinas (especialmente IL-1β, IL-6, IL-10, IFN-γ, TNF-α y TGF-β) involucra factores asociados con trastornos psiquiátricos. La neuroinflamación, disrupción de la barrera hematoencefálica, invasión periférica de células inmunes en el sistema nervioso central, deterioro de la neurotransmisión, disfunción del eje hipotálamo-hipófisis suprarrenal (HPA), activación de la microglía y la inducción de indoleamina 2,3-dioxigenasa (IDO), representan interacciones entre las vías de los sistemas inmunes y el mecanismo psicopatológico que sustentan los trastornos psiquiátricos.
Los pacientes ambulatorios mostraron mayor incidencia de ansiedad y trastornos del sueño, mientras que, contrario a lo esperado, la duración de la hospitalización se correlacionó inversamente con los síntomas de TEPT, depresión, ansiedad y OC.
Los hallazgos aumentarán las preocupaciones sobre los efectos psicológicos del virus. El estudio afirma que el TEPT, la depresión mayor y la ansiedad son condiciones no transmisibles asociadas con años de vida vividos con discapacidad. Los autores recomiendan por tanto evaluar la psicopatología de los sobrevivientes de COVID-19 y profundizar la investigación sobre los biomarcadores de inflamación, para diagnosticar y tratar afecciones psiquiátricas emergentes.
El estudio comenta que sus hallazgos reflejan los de estudios anteriores en brotes de coronavirus, incluido SARS, donde las morbilidades psiquiátricas oscilaban entre 10% y 35% en la etapa posterior a la enfermedad.
Las secuelas psiquiátricas y otras secuelas de la enfermedad COVID-19 han sido descritas previamente aquí: https://megalabs.global/conexion_old_tablas/covid-19-la-enfermedad-secuelas/.
El artículo completo está disponible aquí
Referencias
1) Mazza, M.; et. al. Anxiety and depression in COVID-19 survivors: role of inflammatory and clinical predictors. Brain, Behavior, and Immunity. Available online 30 July 2020. https://doi.org/10.1016/j.bbi.2020.07.037
Consecuencias Psiquiátricas

Ecología y economía para la prevención de pandemias.
Science 24 Jul 2020: Vol. 369, Issue 6502, pp. 379-381
DOI: 10.1126/science.abc3189
Durante un siglo, dos nuevos virus por año han escapado de sus huéspedes naturales a los humanos. Las epidemias MERS, SARS y H1N1 2009, y las pandemias de VIH y enfermedad por coronavirus 2019 (COVID-19), dan testimonio de su daño. Los virus zoonóticos infectan a las personas directamente, con mayor frecuencia cuando manejan primates vivos, murciélagos y otros animales salvajes (o su carne) o indirectamente de animales de granja como pollos y cerdos. Los riesgos son más altos que nunca ya que las asociaciones cada vez más íntimas entre los humanos y los reservorios de enfermedades de la vida silvestre aceleran el potencial de propagación de virus a nivel mundial. Aquí, evaluamos el costo de monitorear y prevenir el contagio de enfermedades debido a la pérdida y fragmentación sin precedentes de los bosques tropicales y al floreciente comercio de vida silvestre. Actualmente, invertimos relativamente poco para prevenir la deforestación y regular el comercio de vida silvestre, a pesar de los planes bien investigados que demuestran un alto retorno de su inversión para limitar las zoonosis y conferir muchos otros beneficios. A medida que el financiamiento público en respuesta a COVID-19 continúa aumentando, nuestro análisis sugiere que los costos asociados de estos esfuerzos preventivos serían sustancialmente menores que los costos económicos y de mortalidad de responder a estos patógenos una vez que hayan surgido.
Reducción de la deforestación
Los bordes de los bosques tropicales son una plataforma de lanzamiento importante para los nuevos virus humanos. Los bordes surgen cuando los humanos construyen caminos o limpian bosques para la producción de madera y la agricultura. Los humanos y su ganado tienen más probabilidades de contactar con la vida silvestre cuando se pierde más del 25% de la cubierta forestal original, y dichos contactos determinan el riesgo de transmisión de enfermedades. La transmisión de patógenos depende de la velocidad de contacto, la abundancia de humanos y ganado susceptible y la abundancia de huéspedes salvajes infectados. Las tasas de contacto varían con el perímetro (la longitud del borde del bosque) entre bosque y no bosque. La deforestación tiende a crear cuadros de ajedrez, con lo cual vemos un perímetro máximo a un nivel de conversión forestal del 50%. A partir de entonces, la abundancia de animales domésticos y humanos supera rápidamente a la de los animales salvajes, por lo que, aunque esperamos que la transmisión disminuya, la magnitud de cualquier brote resultante es mayor. La fragmentación del hábitat complica esto porque aumenta la longitud del perímetro. La construcción de carreteras, los campos de minería y tala, la expansión de centros urbanos y asentamientos, la migración y la guerra, y los monocultivos de ganado y cultivos han llevado a un aumento de la propagación de virus. La caza, el transporte, la agricultura y el comercio de vida silvestre por alimentos, mascotas y medicina tradicional componen estas rutas de transmisión y siguen de cerca la deforestación. Por ejemplo, los murciélagos son los reservorios probables de Ébola, Nipah, SARS y el virus de COVID-19. Los murciélagos frugívoros (Pteropodidae en el Viejo Mundo, el género Artibeus en el Nuevo Mundo) tienen más probabilidades de alimentarse cerca de los asentamientos humanos cuando se alteran sus hábitats forestales; este ha sido un factor clave en la aparición de virus en África occidental, Malasia, Bangladesh y Australia.
El claro vínculo entre la deforestación y la aparición de virus sugiere que un gran esfuerzo para mantener la cubierta forestal intacta tendría un gran retorno de la inversión, incluso si su único beneficio fuera reducir los eventos de emergencia de virus. El ejemplo a mayor escala de reducción de la deforestación dirigida proviene de Brasil entre 2005 y 2012. La deforestación en la Amazonía se redujo en un 70%, pero la producción de la cosecha de soja dominante en la región aún aumentó. Las contribuciones internacionales, complementadas por un Fondo Amazónico, de aproximadamente $ 1 mil millones respaldaron la zonificación del uso de la tierra, las restricciones de mercado y de crédito, y el monitoreo satelital de última generación. El programa de Brasil redujo la fragmentación y el límite de los bosques a un costo menor que el que podría haberse logrado con los enfoques de fijación de precios del carbón.
Existen varias estimaciones de la efectividad y el costo de las estrategias para reducir la deforestación tropical. Con un costo anual de $ 9.6 mil millones, los pagos directos de protección forestal para compensar económicamente la deforestación podrían lograr una reducción del 40% en las áreas con mayor riesgo de propagación de virus. Múltiples programas de pago por servicios ecosistémicos demuestran la efectividad de este enfoque. En el extremo inferior, la adopción generalizada del modelo de política anterior de Brasil podría lograr la misma reducción por solo $ 1.5 mil millones anuales al eliminar los subsidios que favorecen la deforestación, restringir la limpieza de tierras privadas y apoyar los derechos territoriales de los pueblos indígenas. Todos requieren motivación nacional y voluntad política. Puede surgir un fuerte apoyo público para políticas similares de prevención de la deforestación en otros países que se están recuperando de la devastación de COVID-19.
Comercio de vida silvestre
La demanda mundial de vida silvestre hace que las personas ingresen a los bosques para recolectar vida silvestre para la venta en los mercados de las zonas urbanas y rurales. En las ciudades, donde las personas tienen diversas opciones de proteínas, la carne de animales silvestres es un lujo comprado para mostrar su estatus, y ocasionalmente por razones culturales. COVID-19 es el enorme precio que la sociedad paga ahora por tales encuentros con especies silvestres.
Los mercados de vida silvestre y el comercio legal e ilegal de vida silvestre ponen en contacto animales salvajes vivos y muertos con cazadores, comerciantes, consumidores y todos los involucrados en este comercio. El comercio sigue la demanda global del consumidor. Estados Unidos es uno de los mayores importadores mundiales de vida silvestre, incluida la industria masiva de mascotas exóticas. Las condiciones de tránsito, la falta de controles de salud en la importación y los almacenes que conservan animales antes y después de la importación son similares a los mercados de animales vivos, todos conducen a la propagación de enfermedades.
Algunos países tienen industrias de cultivo de vida silvestre destinadas a evitar la caza excesiva de especies silvestres al tiempo que satisfacen las demandas del mercado de proteínas y apelan a las tradiciones culturales. En China, la agricultura de vida silvestre es una industria de US$ 20 mil millones que emplea a unos 15 millones de personas. Con el anuncio de febrero de 2020 por el Comité Permanente del Congreso Nacional del Pueblo sobre la prohibición del consumo de vida silvestre para alimentos y el comercio relacionado en China, hay discusiones en curso sobre la eliminación gradual de esta industria. La justificación es que crea riesgos para la aparición de enfermedades y que las normas de salud y seguridad asociadas con la cría de animales salvajes a menudo son insuficientes. Las leyes para prohibir el comercio nacional e internacional de especies de reservorios de enfermedades de alto riesgo, y la voluntad de mantener su aplicación, son medidas necesarias y precautorias para prevenir la enfermedad zoonótica. Las regulaciones deben mantener a los primates, murciélagos, pangolines, civetas y roedores fuera de los mercados.
Convenios internacionales como la Convención sobre el Comercio Internacional de Especies Amenazadas de Fauna y Flora (CITES) abordan solo una parte del problema. Ellos, las redes regionales y las agencias nacionales que monitorean el comercio de vida silvestre y hacen cumplir las regulaciones carecen de financiación. Las redes regionales de aplicación de la vida silvestre (WEN) podrían fortalecerse para formar parte de una frontera de respuesta efectiva a la futura prevención de pandemias. El presupuesto anual de un WEN, patrocinado por la Asociación de Naciones del Sudeste Asiático, es de US$ 30,000. El presupuesto anual de la CITES es de solo US$ 6 millones. Su secretaría ha declarado recientemente que las enfermedades zoonóticas están fuera del mandato de la CITES; ciertamente están fuera de su presupuesto actual. Ayudar a prevenir el próximo brote podría incluir aumentar los presupuestos de las WEN para las respuestas regionales y, al mismo tiempo, desarrollar protocolos coordinados globalmente para aumentar la capacidad de las WEN en la detección de la salud de la vida silvestre. Aunque no existe una agencia global con la misión de vigilar el comercio de vida silvestre, estimamos los costos de tal esfuerzo considerando el presupuesto operativo anual de la Organización Mundial de Sanidad Animal (OIE), que tiene la misión de evaluar el riesgo de enfermedad en el comercio de ganado sin realizar pruebas. Luego agregamos los costos de la vigilancia de enfermedades a gran escala en la vida silvestre, ajustados al volumen global del comercio de vida silvestre.
La restricción del acceso a la vida silvestre para la alimentación y otros usos debe considerar a los pueblos indígenas y aquellos en comunidades remotas para quienes la vida silvestre proporciona proteínas esenciales. En algunas partes del mundo, la dependencia de la vida silvestre migratoria como el caribú y el salmón motiva la administración de grandes extensiones de hábitat. Aunque se debe mantener el derecho a las dietas tradicionales, las personas pueden estar en riesgo de cosechar vida silvestre. Estos son problemas de seguridad alimentaria que los gobiernos y las agencias de desarrollo deben enfrentar. Cuando sea necesario, deben incluir educación y conciencia sobre el manejo de animales, el saneamiento y la transmisión de enfermedades, así como el manejo sostenible de la vida silvestre y el apoyo para desarrollar alimentos alternativos a nivel de aldea. La caza y comercialización legal de la vida silvestre que cumple con los requisitos nutricionales básicos de manera sostenible puede regularse para reducir el riesgo de pandemias emergentes. Con el tiempo, las medidas culturalmente sensibles podrían garantizar el acceso de los pueblos indígenas a dietas saludables y reducir los riesgos de pandemia.
Detección temprana y control
Existe un subregistro sustancial de exposición a enfermedades zoonóticas. Corregir esto proporcionaría grandes oportunidades para la prevención. El virus Nipah se descubrió en 1998, originándose en murciélagos frutales, y causó un brote masivo de enfermedades respiratorias en cerdos y encefalitis letal en personas en Malasia. La vigilancia centinela en los hospitales de Bangladesh reveló múltiples grupos de casos anuales y brotes con una tasa promedio de letalidad del 70%.
Del mismo modo, el SARS y COVID-19 surgieron como brotes de enfermedades respiratorias en Guangdong y Wuhan, China, respectivamente. Las encuestas serológicas de personas en la provincia rural de Yunnan mostraron que el 3% tenía anticuerpos contra especies de virus similares de su reservorio principal, los murciélagos de herradura (Rhinolophus spp.).
Para cuantificar y reducir el riesgo de propagación de patógenos se requiere un descubrimiento viral en la vida silvestre y pruebas de poblaciones humanas y ganaderas en regiones de alto riesgo de aparición de enfermedades. Por ejemplo, el programa Wellcome Trust VIZIONS evaluó la vida silvestre, los humanos y el ganado en busca de patógenos conocidos en las zonas rurales de Vietnam. El proyecto PREDICT de la Agencia de los Estados Unidos para el Desarrollo Internacional (USAID) analizó la propagación de virus en personas con alto contacto con la vida silvestre en 31 países. PREDICT incluyó programas de educación comunitaria para crear conciencia sobre el riesgo zoonótico y reducir el contacto con la vida silvestre. Trabajó para evitar el contagio mediante la identificación de comportamientos de alto riesgo y utilizó encuestas serológicas para examinar patrones estacionales de riesgo. Las intervenciones incluyeron el uso de faldas de bambú para reducir la contaminación de la savia de la palma por el virus Nipah, una mayor bioseguridad en las granjas ganaderas para reducir el contacto entre la vida silvestre, el ganado y el ser humano, la promoción del lavado de manos y el uso de equipos de protección personal cuando están en contacto cercano con la vida silvestre. Redujo la capacidad de la vida silvestre para eliminar virus en las interfaces al cerrar cuevas de murciélagos de alto riesgo.
Los costos de las medidas para prevenir el derrame varían. PREDICT de USAID gastó $ 200 millones en 10 años. Este costo se compara favorablemente con los $ 1.2 mil millones para el Proyecto Global Virome, un proyecto de 10 años diseñado para identificar el 70% de los virus potencialmente zoonóticos desconocidos en la vida silvestre a nivel mundial. Aunque tenemos pruebas de concepto para el descubrimiento de enfermedades con potencial de emergencia, para la identificación de efectos secundarios activos y para programas que reducen el riesgo, se necesita investigación para cuantificar el retorno de la inversión para estos programas. Los programas piloto deben priorizar los indicadores que permiten una mejor evaluación de los costos y beneficios de la reducción de riesgos (ver SM).
Después del derrame, una segunda ventana de oportunidad crítica es la prevención de brotes más grandes (2). Los primeros casos de VIH / SIDA, síndrome pulmonar por hantavirus, virus Nipah, SARS y COVID-19 no se detectaron durante semanas, meses o años (VIH) antes de la identificación del patógeno. Los retrasos en la identificación han disminuido, pero esto varía geográficamente. En los países de bajos ingresos, los grandes brotes con mortalidad sustancial a menudo no se diagnostican, especialmente cuando los síntomas imitan a los de otras enfermedades conocidas. Se están llevando a cabo proyectos piloto en clínicas de muchas regiones rurales para identificar la etiología de los casos con síntomas similares (vigilancia sindrómica). Por ejemplo, un proyecto piloto que costó $ 200,000 por año para la vigilancia sindrómica del virus Nipah en hospitales de Bangladesh resultó en un aumento del factor 3 en la detección de eventos de contagio (13). El Instituto Nacional de Alergias y Enfermedades Infecciosas de EE. UU. Está lanzando una serie de Centros de Investigación en Enfermedades Infecciosas Emergentes. Se espera que los contratos para este trabajo sean de $ 1.5 millones por año, centrándose en zoonosis virales específicas de alto riesgo en puntos críticos de enfermedades emergentes. Los programas de detección y control dirigidos a brotes en sus primeras etapas resultarían en ahorros considerables al reducir la morbilidad y la mortalidad. Una prioridad es identificar indicadores de reducción de riesgos a medida que se implementan los programas piloto y calcular los costos, los ahorros de costos y los beneficios de expandirlos.
Copmercio de animales de granja
El ganado es reservorio crítico y enlace en enfermedades emergentes. La influenza H5N1 se encontró con la interfaz humano-vida silvestre (aves silvestres → aves de corral → cadena de transmisión humana), al igual que la influenza H1N1 (aves → cerdo → humanos). Muchos brotes relacionados con el ganado han alcanzado la cúspide de la aparición de una pandemia, como el virus Nipah (murciélago de la fruta → cerdo → humano) y el coronavirus del síndrome de diarrea aguda porcina (murciélago → cerdo) (14). Estos enlaces son bien reconocidos y son el foco de los paquetes de prevención de pandemias propuestos por el Congreso de los Estados Unidos (H.R.3771). Existen planes de salud veterinaria bien establecidos, como el programa de intervención de bioseguridad agrícola One World One Health del Banco Mundial, diseñado para reducir el riesgo de influenza H5N1. Con costos de decenas de miles de millones de dólares, las propuestas que se ocupan del papel del ganado en las pandemias se encuentran entre las más avanzadas y ambiciosas de las que se consideran seriamente. Hemos conocido estos riesgos por más tiempo (por ejemplo, influenza) y podemos controlar la bioseguridad de la granja más fácilmente que la vida silvestre.
Conclusiones
Las acciones que describimos pueden ayudar a prevenir futuras pandemias zoonóticas antes de que comiencen. El monitoreo por sí solo generaría ahorros sustanciales de costos, incluso en el contexto de brotes pandémicos mucho menos graves que COVID-19. Los costos brutos estimados de las acciones que proponemos suman un total de US$ 22 a US$ 31 mil millones por año. La reducción de la deforestación tiene el beneficio adicional de alrededor de US$ 4 mil millones por año en beneficios sociales de las emisiones reducidas de gases de efecto invernadero, por lo que los costos netos de prevención oscilan entre US$ 18 y US$ 27 mil millones por año. En comparación, COVID-19 nos ha demostrado el inmenso costo potencial de una pandemia. El mundo puede perder al menos US$ 5 millones de millones en PIB en 2020, y la disposición a pagar por las vidas perdidas constituye muchos billones adicionales (ver SM). Estos costos excluyen el aumento de la morbilidad, las muertes por otras causas debido a la alteración de los sistemas médicos y la pérdida para la sociedad de las actividades que no se realizan debido al distanciamiento social.
Para justificar los costos de la prevención, el valor de un año de estas estrategias preventivas solo necesitaría reducir la probabilidad de otra pandemia como COVID-19 en el próximo año en aproximadamente un 27% por debajo de la probabilidad de referencia en el escenario más probable, incluso ignorando los beneficios auxiliares de secuestro de carbono. Exploramos ocho escenarios alternativos con suposiciones variadas extraídas de los valores más altos y más bajos tanto de costos de prevención como de daños pandémicos, y asumiendo que las pandemias extremas ocurren una vez cada 100 años o una vez cada 200 años. En todos los escenarios menos uno, la prevención solo necesita reducir la probabilidad de una pandemia en menos de la mitad, y en un caso la reducción de probabilidad de porcentaje de equilibrio es tan baja como 12%. Estimamos que el valor actual de los costos de prevención durante 10 años es solo alrededor del 2% de los costos de la pandemia de COVID-19.
Reconocemos que no hemos proporcionado más que un bosquejo de los componentes clave de un conjunto económicamente factible de estrategias ecológicas de prevención de pandemias. Los límites en la disponibilidad de información limitan nuestra capacidad de realizar un análisis más exhaustivo. En cambio, contamos la información fácilmente disponible para evaluar la probabilidad de que una inversión de los costos de la prevención de pandemias produzca beneficios netos positivos para el mundo. Nuestros cálculos son conservadores en la dirección de hacer que sea difícil encontrar que la prevención probablemente valga la pena, y sin embargo ese es nuestro hallazgo. Los estudios futuros podrían reducir las incertidumbres en los costos y la eficacia de esas estrategias y determinar el conjunto de acciones más rentable. Un análisis completo de costo-beneficio de la prevención de pandemias podría rastrear los flujos de costos de prevención a lo largo del tiempo, permitir dependencias intertemporales y modelar las pandemias prevenidas como productos de una distribución de eventos de enfermedades que no son tan graves como COVID-19. Nuestros hallazgos dejan en claro que este esfuerzo de investigación está justificado, porque los beneficios netos de detener las pandemias antes de que comiencen podrían ser enormes.
Reconocemos que a medida que el mundo emerge de la pandemia de COVID-19, las prioridades económicas pueden cambiar para hacer frente a las crecientes demandas del desempleo, las enfermedades crónicas, las bancarrotas y las graves dificultades financieras de las instituciones públicas. Sin embargo, existe evidencia sustancial de que la tasa de aparición de nuevas enfermedades está aumentando y que sus impactos económicos también están aumentando. Posponer una estrategia global para reducir el riesgo de pandemia conduciría a un aumento continuo de los costos. Dado el aluvión de costosas enfermedades emergentes en los últimos 20 años, instamos a que el estímulo y otros fondos de recuperación incluyan las estrategias que hemos establecido para reducir el riesgo de pandemia. La sociedad debe esforzarse por evitar algunos de los impactos de futuras pandemias.
Ecología y economía para la prevención de pandemias

¿Cómo el SARS-CoV-2 causa COVID-19?
Los virus ingresan a las células e inician la infección al unirse a sus receptores de superficie celular afines. La expresión y distribución de los receptores de entrada viral regulan su tropismo, determinando los tejidos que están infectados y, por lo tanto, la patogénesis de la enfermedad. El coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) es el tercer coronavirus humano conocido por cooptar la enzima convertidora de angiotensina peptidasa 2 (ACE2) para la entrada celular. La interacción entre SARS-CoV-2 y ACE2 es crítica para determinar tanto el tropismo tisular como la progresión de la infección temprana por SARS-CoV-2 a la enfermedad grave por coronavirus 2019 (COVID-19). Comprender la base celular de la infección por SARS-CoV-2 podría revelar tratamientos que previenen el desarrollo de enfermedades graves y, por lo tanto, reducen la mortalidad.
Al igual que con todos los coronavirus, la entrada de células SARS-CoV-2 depende de su proteína espiga (S) de 180 kDa, que media dos eventos esenciales: unión a ACE2 por la región amino-terminal, y fusión de membranas virales y celulares a través de la región carboxilo terminal. La infección de las células pulmonares requiere la activación proteolítica del huésped de la espiga en un sitio de escisión de furina polibásico. Hasta la fecha, este sitio de escisión se encuentra en todas las proteínas de pico de aislados clínicos de SARS-CoV-2, así como en algunos otros virus altamente patógenos (p. Ej., Influenza aviar A), pero está ausente del SARS-CoV y es probable que haya sido adquirido por recombinación entre coronavirus en murciélagos. La escisión por la proteina furina, por lo tanto, expande el tropismo celular del SARS-CoV-2 y puede haber facilitado la transmisión de los murciélagos a los humanos (1). La fusión de membrana también requiere la escisión por proteasas adicionales, particularmente la proteasa transmembrana serina 2 (TMPRSS2), una proteasa de la superficie de la célula huésped que corta la espiga poco después de unirse a ACE2 (3). El tropismo por SARS-CoV-2, por lo tanto, depende de la expresión de proteasas celulares, así como de ACE2.
También están surgiendo otras proteínas que permiten la entrada de células SARS-CoV-2, incluida la neuropilina 1 (NRP1), un receptor que se une al extremo carboxilo terminal en la espiga que se expone después de la escisión de la furina. No está claro cómo NRP1 promueve la entrada celular, pero puede aumentar aún más los tipos de células infectadas.
De los siete coronavirus humanos conocidos, tres son altamente patógenos [SARS-CoV, SARS-CoV-2 y Síndrome respiratorio del Medio Oriente (MERS) -CoV], y los cuatro restantes (HCoV-NL63, HCoV-229E. HCoV-OC43 y HCOV-HKU1) son menos virulentos y causan «resfriados comunes». SARS-CoV, SARS-CoV-2 y HCoV-NL63 usan ACE2 como su receptor de entrada celular. MERS-CoV se une a DPP4 (dipeptidil peptidasa 4) y HCoV-229E usa CD13 (aminopeptidasa N) (2). No se han identificado receptores de proteínas del huésped para los otros dos virus. Parece una coincidencia notable que todos los receptores de coronavirus humanos conocidos son peptidasas de la superficie celular, particularmente porque las interacciones no involucran el sitio activo de endopeptidasa. La presencia de una región específica dentro de ACE2, dirigida por tres coronavirus, es particularmente notable. Por el contrario, el dominio de unión al receptor de la espiga está codificado por la parte más variable del genoma del coronavirus. Esto implica que la diversificación de estos virus generó diferentes secuencias que convergieron en la misma región de la misma proteína utilizando soluciones estructurales alternativas. Entonces, ¿qué tiene de especial ACE2?
ACE2 es una proteína transmembrana mejor caracterizada por su papel homeostático en contrarrestar los efectos de ACE en el sistema cardiovascular. ACE convierte la angiotensina I en angiotensina II, un octapéptido altamente activo que exhibe tanto efecto vasopresor (contracción vascular para aumentar la presión arterial) como actividades proinflamatorias. La actividad carboxipeptidasa de ACE2 convierte la angiotensina II en el heptapéptido angiotensina- (1-7), un antagonista funcional de la angiotensina II. Debido a que la ECA se expresa altamente en las células endoteliales vasculares de los pulmones, es probable que la angiotensina II también sea alta en la vasculatura pulmonar. De hecho, la eliminación de Ace2 en modelos de ratón de lesión pulmonar aguda da como resultado una enfermedad más grave, lo que sugiere un papel protector para ACE2 en el tejido pulmonar. En muchas interacciones virus-huésped, la expresión del receptor viral está regulada negativamente en las células infectadas, y la expresión de ACE2 en los pulmones de los ratones se redujo por la infección por SARS-CoV. Por lo tanto, el agotamiento de ACE2 puede desempeñar un papel causal en la lesión pulmonar causada por el SARS-CoV y el SARS-CoV-2, y se informa angiotensina II en plasma alto en pacientes con COVID-19. Sin embargo, MERS-CoV causa una enfermedad pulmonar similar sin apuntar a ACE2, por lo que otros factores también deben ser importantes.
Como virus respiratorio, el SARS-CoV-2 debe ingresar inicialmente a las células que recubren el tracto respiratorio. La secuenciación de células individuales y el mapeo in situ de ARN del tracto respiratorio humano muestran que la expresión de ACE2 y TMPRSS2 es más alta en las células epiteliales nasales ciliadas, con menores cantidades en las células epiteliales bronquiales ciliadas y las células epiteliales alveolares tipo II. Esto se traduce en una mayor permisividad de las células epiteliales del tracto respiratorio superior versus inferior para la infección por SARS-CoV-2 in vitro y se adapta a la patología de la enfermedad: los síntomas del tracto respiratorio superior son comunes temprano en la enfermedad, con hisopos nasofaríngeos y de garganta positivos para el SARS-CoV-2 en presentación clínica. A diferencia del SARS-CoV, la infectividad de los pacientes con SARS-CoV-2 alcanza su punto máximo antes del inicio de los síntomas. De hecho, la transmisión presintomática hace que el SARS-CoV-2 sea imposible de contener a través del aislamiento del caso solo y es un factor clave de la pandemia. Esta alteración en el patrón de la enfermedad puede relacionarse con la adquisición del sitio de escisión de la furina en la espiga o el aumento de la afinidad de unión por ACE2 en SARS-CoV-2, en comparación con el SARS-CoV.
Si el papel principal de ACE2 es escindir la angiotensina II, no está claro por qué la expresión en el tejido pulmonar es más prominente en las células epiteliales que en las endoteliales. Además, el Human Cell Atlas destaca la expresión de ACE2 en los enterocitos intestinales, en lugar de en los pulmones. Esta distribución puede reflejar funciones no enzimáticas de ACE2, como el chaperón de transportadores de aminoácidos. De hecho, la infección por SARS-CoV-2 del tracto gastrointestinal (GI) es común, con ARN viral detectable en las heces en hasta el 30% de los pacientes con COVID-19. Esto probablemente contribuye a la frecuencia de los síntomas gastrointestinales. Por el contrario, aunque se cree que la transmisión fecal-oral de coronavirus es prominente entre los murciélagos, parece ser una ruta de transmisión menor para el SARS-CoV-2 en humanos, tal vez porque el líquido del colon inactiva el virus. No está claro si la expresión extrapulmonar de ACE2 y la infección viral concomitante explican otras manifestaciones clínicas de SARS-CoV-2. La asociación entre la infección por SARS-CoV-2 y la anosmia (pérdida del olfato) puede reflejar la expresión de ACE2 y TMPRSS2 en células sustentaculares, que mantienen la integridad de las neuronas sensoriales olfativas. Las células epiteliales olfativas también expresan NRP1 y podrían proporcionar una ruta directa al cerebro.
Aunque una proporción sustancial de individuos infectados con SARS-CoV-2 informan pocos síntomas, si es que los hay, y se recuperan por completo, la tomografía computarizada (TC) de tórax presenta evidencia de neumonitis viral en> 90% de los casos sintomáticos dentro de los 3 a 5 días posteriores al inicio. Presumiblemente, esto refleja la replicación viral en el tracto respiratorio inferior, con infección de neumocitos tipo II e inflamación acompañante (ver la figura). La patología pulmonar en esta fase temprana se informa poco porque la mayoría de los pacientes se recuperan. La histopatología de monos cynomolgus, 4 días después de la inoculación con SARS-CoV-2, muestra una neumonitis viral con edema alveolar, fuga capilar, infiltración celular inflamatoria, engrosamiento intersticial y fusión celular (una característica de la infección por coronavirus), con expresión de pico viral en células epiteliales alveolares.
Alrededor del 80% de los pacientes con neumonitis por COVID-19 se recuperan sin tratamiento específico. Sin embargo, alrededor del 20% de los pacientes se deterioran, a menudo rápidamente, entre 7 y 10 días después del inicio de los síntomas. Aquí es cuando los pacientes ingresan con mayor frecuencia en el hospital, con empeoramiento de la fiebre, hipoxia, linfopenia, marcadores inflamatorios en aumento [proteína C reactiva (PCR), interleucina-1 (IL-1) e IL-6], coagulopatía y afectación cardiovascular. Alrededor del 25% de estos pacientes requerirán ventilación mecánica, lo que se asocia con una alta mortalidad (50 a 80%). La demografía de este grupo «de riesgo» se reproduce en muchos países: hombres mayores con hipertensión, diabetes y obesidad, así como una contribución de etnia menos bien definida. Factores similares regulan la expresión de ACE2, lo que puede contribuir a la gravedad de la enfermedad. No obstante, la cantidad y distribución de la expresión de ACE2 no puede ser el único factor que afecta la progresión de la enfermedad, porque los tres coronavirus humanos que usan ACE2 para la entrada en las células exhiben una patogenicidad marcadamente diferente.
¿Qué causa el deterioro agudo que conduce a COVID-19 severo? La patología pulmonar en la enfermedad grave es diferente de la neumonitis anterior, con pérdida progresiva de integridad epitelial-endotelial, lesión capilar septal y una marcada infiltración de neutrófilos, con depósito de complemento, depósito de antígeno viral intravascular y coagulación intravascular localizada. Si la neumonitis viral anterior refleja la infección directa mediada por ACE2 de los neumocitos tipo II, ¿qué impulsa esta próxima fase potencialmente mortal de lesión pulmonar aguda, con la ruptura concomitante de la barrera epitelial respiratoria, daño endotelial y deterioro del paciente? Lo más importante: ¿cómo se puede detener?
El momento del deterioro sugiere un papel para el sistema inmunitario adaptativo, ya sea anticuerpos o células T, y tiene muchas características distintivas de la inflamación inmunitaria. La lesión endotelial puede ser el resultado del daño mediado por el sistema inmunitario, a través de la activación del complemento, la mejora dependiente de anticuerpos y / o la liberación de citocinas. Por lo tanto, la atención se ha centrado en el uso de terapias inmunomoduladoras en pacientes con enfermedad grave. Sin embargo, el culpable más obvio de una enfermedad grave es el virus en sí, ya sea solo o con patología inmune. La ruptura de la barrera epitelial-endotelial pulmonar podría desencadenar daño endotelial y diseminación viral, con una infección más generalizada. Los estudios que documentan el curso temporal del desprendimiento de ARN del SARS-CoV-2 se limitan principalmente a la enfermedad leve y generalmente muestran una disminución progresiva después de un pico en torno al inicio de los síntomas. Sin embargo, la carga viral de los hisopos pulmonares puede correlacionarse con la gravedad de la enfermedad, y los pacientes con enfermedad pulmonar grave siguen siendo ARN positivos por más tiempo. Es fundamental determinar cuánto tiempo persiste realmente la replicación viral activa en los pulmones de pacientes con enfermedad grave, y con qué frecuencia se produce la replicación viral en sitios extrapulmonares donde se expresa ACE2 (u otros receptores), como el endotelio vascular.
Aunque existen grandes esfuerzos para comprender y tratar el COVID-19 grave, sería preferible prevenir el desarrollo y la progresión de la enfermedad clínica. ¿Cómo se puede lograr esto? Los candidatos a vacunas están dirigidos principalmente a la obtención de anticuerpos neutralizantes, para evitar la unión de la proteína espiga a ACE2. El mismo fundamento sustenta el uso de la inmunización pasiva, con plasma convaleciente o anticuerpos monoclonales, o la administración de ACE2 recombinante soluble. Alternativamente, se pueden usar medicamentos antivirales para atacar enzimas virales esenciales como la ARN polimerasa dependiente de ARN.
La experiencia de otras infecciones, como la influenza, enfatiza que el tratamiento con agentes antivirales es más efectivo cuando se administra lo antes posible en la infección. Por lo tanto, es esencial identificar a las personas con infección temprana por SARS-CoV-2 que tienen un alto riesgo de progresión a enfermedad grave, y probar terapias antivirales para prevenir la entrada y replicación viral. No debería ser demasiado difícil identificar a estos pacientes «en riesgo» que están en peligro de progresar a una enfermedad grave a través del rastreo y las pruebas de contacto, incluso antes del inicio de los síntomas. Por el contrario, retrasar el tratamiento antiviral hasta que los pacientes sean hospitalizados con una lesión pulmonar grave puede ser demasiado tarde, y es probable que se requiera una combinación con modulación inmune.
Cómo el SARS-CoV-2 causa COVID-19

La FDA autoriza las primeras pruebas que estiman los anticuerpos en pacientes con infección previa por SARS-CoV-2
El 31 de Julio de 2020, la FDA autorizó las dos primeras pruebas serológicas de COVID-19 que muestran la cantidad estimada de anticuerpos presentes en la sangre del individuo (1). Los tests son de Siemens, siendo estos ADVIA Centaur COV2G (2) y Atellica COV2G (3). Son tests cualitativos y semicuantitativos, lo que significa que no muestran una medición precisa, sino que estiman la cantidad de anticuerpos de un paciente producidos contra la infección con el virus SARS-CoV-2.
El ensayo ADVIA Centaur® SARS-CoV-2 IgG (COV2G) es un inmunoensayo quimioluminiscente destinado a la detección de anticuerpos IgG contra SARS-CoV-2 en suero y plasma humanos (EDTA de potasio y heparina). El ensayo está destinado a utilizarse como una ayuda en la identificación de individuos con una respuesta inmune adaptativa a SARS-CoV-2, que indica infección reciente o previa. En este momento se desconoce por cuánto tiempo persisten los anticuerpos después de la infección y si la presencia de anticuerpos confiere inmunidad. El ensayo no debe utilizarse para diagnosticar infección aguda por SARS-CoV-2. Los anticuerpos IgG contra el SARS-CoV-2 son generalmente detectables en sangre varios días después de la infección inicial, aunque la duración en el tiempo de los anticuerpos después de la infección no está bien caracterizada. Los resultados negativos no excluyen la infección aguda por SARS-CoV-2. Si se sospecha infección aguda, es necesario realizar pruebas directas para el SARS-CoV-2. Los resultados falsos positivos para el ensayo pueden ocurrir debido a reactividad cruzada de anticuerpos preexistentes u otras causas. (2) El ensayo Atellica® IM SARS-CoV-2 IgG (COV2G) es también es un inmunoensayo quimioluminiscente para la detección cualitativa y semicuantitativa de IgG contra SARS-CoV-2 en humanos suero y plasma (EDTA de potasio y heparina de litio) con el analizador de IM Atellica®. (3)
Tim Stenzel, director de la Oficina de Diagnóstico in vitro y Salud Radiológica en el Centro de Dispositivos y Salud Radiológica de la FDA afirmó que un mayor conocimiento sobre estos anticuerpos puede esclarecer acerca de la inmunidad potencial a la enfermedad. Agregó que los pacientes que los muestran no deben interpretar que sean inmunes o tengan algún nivel de inmunidad contra el virus. (1)
La FDA advierte a los pacientes que no usen los resultados de estas pruebas como una indicación de que pueden dejar de tomar medidas para protegerse y proteger a otros, detener el distanciamiento social, dejar de usar máscaras o volver al trabajo. La FDA recuerda también a los pacientes que las pruebas serológicas no deben usarse para diagnosticar una infección activa, ya que solo detectan anticuerpos que el sistema inmunitario desarrolla en respuesta al virus, no detectando al virus per se. (1)
Referencias:
FDA tests detección anticuerpos
Los fabricantes de drogas europeos Sanofi y GSK llegan a un acuerdo de US$ 2,1 mil millones con los EE. UU. por una vacuna contra el coronavirus
El gobierno federal anunció el viernes un acuerdo de US$ 2.1 mil millones con la compañía farmacéutica francesa Sanofi y su socio británico, GSK, para apoyar el desarrollo de una vacuna contra el coronavirus en la que las compañías están trabajando juntas.
El contrato, el más grande del gobierno de EE. UU. firmado hasta ahora, incluye la entrega de 100 millones de dosis para los Estados Unidos y es parte de la operación Warp Speed, la iniciativa de la administración Trump para acelerar el desarrollo de vacunas, tratamientos y diagnósticos para el coronavirus.
Estados Unidos ahora ha comprometido más de US$ 8 mil millones para apoyar el desarrollo de vacunas, o la precompra de dosis, de Sanofi y GSK, Johnson & Johnson, Moderna, Novavax, Pfizer y AstraZeneca.
Se espera que la primera prueba en humanos de la vacuna experimental comience en septiembre, con ensayos más grandes para probar su efectividad que esperan comenzar antes de fin de año. Las compañías anticipan tener suficientes datos para buscar una decisión regulatoria en la primera mitad de 2021 y planean fabricar mil millones de dosis por año.
«La necesidad global de una vacuna para ayudar a prevenir el covid-19 es enorme, y ninguna vacuna o compañía por sí sola podrá satisfacer la demanda global», dijo Thomas Triomphe, responsable global de Sanofi Pasteur, en un comunicado.
El contrato, que incluye la opción de que Estados Unidos compre 500 millones de dosis adicionales, incluye apoyo para el desarrollo clínico de la vacuna y un acuerdo de compra anticipada. El gobierno de los Estados Unidos ha comprometido miles de millones de dólares a las empresas para reducir los riesgos financieros de fabricar vacunas antes de que los fabricantes de medicamentos sepan si funcionan.
«La cartera de vacunas que se está armando para la Operación Warp Speed aumenta las probabilidades de que tengamos al menos una vacuna segura y efectiva tan pronto como finalice este año», dijo el secretario de Salud y Servicios Humanos, Alex Azar, en un comunicado.
La mayoría de los expertos dicen que serán necesarias varias vacunas para satisfacer la demanda mundial y Estados Unidos ha invertido en múltiples tecnologías. Pero la inversión masiva de los contribuyentes ha generado preocupaciones sobre si las vacunas fuertemente subsidiadas por el gobierno tendrán un precio justo. A medida que los países ricos se esfuerzan por reservar dosis de vacunas, también existe la preocupación de que éstos monopolicen los productos necesarios para proteger a las personas en todo el mundo.
Además del acuerdo con Estados Unidos, Sanofi y GSK llegaron a un acuerdo a principios de semana para proporcionar 60 millones de dosis al Reino Unido y están cerca de un acuerdo para proporcionar 300 millones de dosis a la Unión Europea.
El viernes, Pfizer anunció que suministraría 120 millones de dosis de su vacuna a Japón en el primer semestre de 2021, pendiente de aprobación regulatoria.
Dependiendo de la geografía del brote cuando las vacunas estén disponibles, los países con menos recursos médicos pueden necesitar la vacuna más que los países ricos.
Sanofi y GSK dijeron en un comunicado que han comprometido una «porción significativa» del suministro total en 2021 y 2022 al Access to COVID‐19 Tools Accelerator, una colaboración global centrada en proporcionar acceso equitativo a las vacunas.
«Las ganancias potenciales con nuestra vacuna se reinvertirán hacia la investigación relacionada con el coronavirus, la preparación para una pandemia a largo plazo y el aumento de la capacidad de fabricación», dijo el portavoz de Sanofi, Nicolas Kressmann.
GSK ha dicho anteriormente que no planea beneficiarse de su programa de vacunas durante la pandemia.
Los fabricantes de drogas europeos Sanofi y GSK llegan a un acuerdo de $ 2,1 mil millones con los EE. UU. por una vacuna contra el coronavirus