El desarrollo de nuevas pruebas de coronavirus que podrían ayudar a poner fin a la pandemia
Los investigadores están luchando para encontrar otras formas de diagnosticar el coronavirus y realizar millones de pruebas por semana, un paso clave para volver a la normalidad.
El momento no podría haber sido peor. En marzo, justo cuando el brote de coronavirus de Tailandia comenzó a aumentar, tres hospitales en Bangkok anunciaron que habían suspendido las pruebas para detectar el virus porque se habían quedado sin reactivos. Los investigadores tailandeses se apresuraron a ayudar a los laboratorios clínicos del país a satisfacer la demanda. En busca de pruebas asequibles y fáciles de usar, el biólogo de sistemas Chayasith (Tao) Uttamapinant en el Instituto de Ciencia y Tecnología Vidyasirimedhi en Rayong contactó a un viejo conocido: el co-descubridor de CRISPR, Feng Zhang, quien había estado desarrollando un ensayo para coronavirus inspirado en la tecnología de edición de genes.
En cuestión de días, Uttamapinant recibió kits del laboratorio de Zhang en el MIT y Harvard en Cambridge, Massachusetts, y los probó en muestras de un hospital en Bangkok. «Los kits son bastante baratos y funcionan bien», dice Uttamapinant, quien espera que la prueba sea aprobada para uso clínico para fin de año. Se ha asociado con bioquímicos en Tailandia para producir los reactivos de prueba localmente, con Zhang en espera de apoyo. «Este esfuerzo para producir todo localmente tendrá un impacto duradero en el monitoreo y diagnóstico de enfermedades infecciosas en esta parte del mundo», dice Uttamapinant.
Los epidemiólogos dicen que las pruebas masivas para el SARS-CoV-2, que requieren millones de pruebas por país por semana, son la forma más práctica de salir de la crisis actual. Permite a los funcionarios aislar a aquellos que dan positivo, limitar la propagación de la enfermedad y ayudar a determinar cuándo es seguro relajar las restricciones.
Pero los países están luchando para aumentar las pruebas. Una razón es que la prueba estándar para detectar SARS-CoV-2, basada en una técnica de laboratorio llamada reacción en cadena de la polimerasa de transcripción inversa o RT-PCR, requiere personal capacitado, suministros químicos específicos e instrumentos costosos que demoran horas en proporcionar resultados y, a menudo, están disponibles solo en laboratorios que brindan servicios de rutina. Esto limita el número de pruebas que se pueden hacer, especialmente en los países en desarrollo. Incluso en regiones ricas como los Estados Unidos, los proveedores han reportado una grave escasez de kits de prueba y materiales requeridos, desde hisopos nasales hasta reactivos químicos, debido a problemas en la cadena de suministro. Ampliar rápidamente las pruebas confiables también ha resultado ser un desafío: las primeras pruebas de RT-PCR desarrolladas por los Centros para el Control y la Prevención de Enfermedades de Estados Unidos funcionaron mal, por ejemplo, lo que provocó una serie de retrasos.
Grupos de investigación en todo el mundo ahora están ideando pruebas que van más allá del PCR.
Se están desarrollando docenas de métodos de diagnóstico, todos los cuales detectan material viral pero de diferentes maneras: algunos son ajustes para RT-PCR que hacen que la prueba sea más rápida o fácil de usar; otros usan la herramienta de edición de genes CRISPR para concentrarse en fragmentos genéticos de SARS-CoV-2; y algunos identifican el virus usando proteínas que se encuentran en su superficie. Muchas de estas pruebas, como las de Zhang, se están validando con muestras clínicas, y algunas ya están en la clínica.
En abril, los Institutos Nacionales de Salud de EE. UU. destinaron 1.500 millones de dólares para el desarrollo de pruebas de coronavirus, con el objetivo de permitir millones de pruebas por semana para fines de este verano. «Cuanto antes podamos encontrar una solución», dice Zhang, «antes podremos reanudar alguna forma de normalidad».
Si esas pruebas están listas pronto, serían buenas noticias para la pandemia actual y para brotes futuros. Muchos de los ensayos en desarrollo podrían adaptarse fácilmente a un patógeno emergente una vez que se decodifique su secuencia genética, dice Isabella Eckerle, viróloga de la Universidad de Ginebra en Suiza. Eckerle dice que, aunque la prueba ideal aún no existe, «hay muchas cosas en en el pipeline que podrían ser útiles».
Más allá del PCR
Las pruebas para el coronavirus se dividen en dos grandes categorías:
1) las que detectan material genético del virus o las moléculas en su superficie, que se utilizan para diagnosticar si una persona tiene una infección activa, y 2) las que detectan la presencia de anticuerpos, revelando si alguien ha sido infectado y ha desarrollado una respuesta inmune al virus. Las pruebas de anticuerpos tienen un uso diagnóstico limitado: si a una persona se le realiza la prueba temprano en el curso de la infección, cuando su respuesta inmune aún se está acumulando, la prueba podría no detectar anticuerpos.
Y debido a que las personas con el coronavirus son más infecciosas al inicio de los síntomas, las pruebas de material viral son cruciales para identificar quién debe estar aislado. En los Estados Unidos, los ensayos de diagnóstico viral representan la mayoría de las pruebas realizadas.
La prueba de diagnóstico “estándar de oro”, que utiliza RT-PCR, funciona buscando en una muestra tomada de células o líquido en la nariz o la garganta de una persona una secuencia genética específica del SARS-CoV-2. Si se encuentra la secuencia viral, la técnica la amplifica a niveles que se pueden detectar. Primero, el virus ARN se convierte en ADN. Luego, las secuencias de ADN de diseño corto conocidas como cebadores realizan varios trabajos. Algunas etiquetan secciones específicas del código genético viral para ayudar a duplicar la secuencia millones de veces, usando un proceso que requiere calentamiento y enfriamiento repetidos. Esta amplificación hace que sea fácil detectar incluso cantidades minúsculas de virus, hasta una sola molécula de ARN por microlitro. Otros cebadores agregan etiquetas a las cadenas de ADN amplificadas. Estas etiquetas liberan una señal fluorescente que es medida por una computadora, señalando la presencia del virus. Las pruebas de RT-PCR estándar para el coronavirus tardan entre una y cuatro horas y pueden tener una precisión de hasta el 100%, aunque la precisión de cualquier prueba de diagnóstico depende de muchos factores, como cuándo se tomó una muestra en el curso de la infección.
Varios enfoques tienen como objetivo reducir el tiempo necesario para obtener un resultado de prueba, como amplificar el ADN a una temperatura constante, lo que elimina la necesidad de múltiples rondas de calentamiento y enfriamiento. Algunos de estos son ensayos existentes que se están personalizando para detectar SARS-CoV-2. Por ejemplo, las compañías estadounidenses de atención médica Cepheid y Abbott han desarrollado ensayos de coronavirus que se ejecutan en plataformas de hardware del tamaño de una tostadora y tardan menos de una hora en realizarse. Sin embargo, los reactivos y las plataformas pueden ser costosos, y Abbott ha advertido que el uso de una solución particular para diluir las muestras de los pacientes puede evitar que su dispositivo detecte el virus.
Varias otras pruebas se basan en una técnica llamada amplificación isotérmica mediada por bucle (LAMP), que también funciona a una temperatura constante y se ha utilizado para identificar virus como el Zika. LAMP se basa en dos enzimas, una para convertir el ARN viral en ADN y otra para copiar el ADN, así como un conjunto de cuatro a seis cebadores cortos diseñados para reconocer diferentes fragmentos del genoma viral. Estos fragmentos no solo ayudan a comenzar la copia, como en RT-PCR, sino que también permiten que las cadenas de ADN recién copiadas formen estructuras en bucle que pueden amplificarse mucho más rápidamente que en la PCR estándar. Sin embargo, es menos preciso y solo se pueden ejecutar unas pocas docenas de muestras a la vez.
Debido a que la técnica no necesita instrumentos especiales, puede usarse en el campo y en regiones que carecen de equipos avanzados, incluidas áreas remotas y campos de refugiados, dice Vicent Pelechano, un experto en genómica del Instituto Karolinska en Estocolmo, quien desarrolló conjuntamente un ensayo basado en LAMP para SARS-CoV-2. «Todo lo que necesitas es un tubo de ensayo que contenga los cebadores, una pipeta, una placa calefactora y una olla de agua», dice. Una sola prueba costaría alrededor de $ 1, sin contar la mano de obra.
En el laboratorio, la prueba basada en LAMP de Pelechano y sus colegas pudo detectar tan solo 10 copias de un genoma de SARS-CoV-2 en no más de 40 minutos. Luego, los investigadores probaron el ensayo utilizando muestras de 248 personas con infección confirmada por coronavirus, y pudieron detectar el virus casi el 90% del tiempo. Pelechano reconoce que la prueba podría resultar menos precisa para algunas muestras, como las contaminadas con sangre.
Pero en algunos lugares, la compensación en precisión podría valer la pena. Los países de bajos ingresos y las zonas devastadas por la guerra no tienen suficientes máquinas de PCR para realizar la prueba de diagnóstico estándar para el coronavirus, dice Nabil Karah, un microbiólogo clínico de la Universidad de Umeå en Suecia. Karah está trabajando con otros científicos y con el equipo de Pelechano para llevar su prueba basada en LAMP a Siria para aumentar la capacidad de prueba local.
Ensayos de aceleración
A principios de marzo, mientras los diagnósticos luchaban por mantenerse al día con la propagación del coronavirus en los Estados Unidos, el ingeniero químico Howard Salis se sintió obligado a ayudar. Para acelerar las pruebas, decidió probar un poderoso enfoque de secuenciación que había revolucionado el ritmo de la investigación genómica. Aproximadamente tres semanas después, el equipo de biólogos sintéticos de Salis en la Universidad Estatal de Pensilvania en University Park encontró una manera de analizar muestras de casi 20,000 personas en una sola corrida.
Su método agrega «códigos de barras moleculares» individuales a las muestras clínicas antes de agruparlas y usar la secuenciación de próxima generación para decodificarlas todas a la vez. Los códigos de barras permiten a los investigadores identificar qué muestras dieron positivo. Otros equipos han publicado detalles de enfoques similares de pruebas en masa, incluida la empresa de nueva creación de biotecnología Octant en Emeryville, California, e investigadores del Broad Institute.
Debido a que los secuenciadores de ADN pueden leer cientos de millones de fragmentos de ADN a la vez, los investigadores estiman que las pruebas basadas en secuenciación podrían usarse para analizar hasta 100,000 muestras en una sola ejecución. Por el contrario, una máquina de PCR estándar puede analizar solo docenas o cientos de muestras al mismo tiempo. Pero estas pruebas de secuenciación toman tiempo, al menos 12 horas, y requieren equipos especializados en instalaciones centralizadas. Obtener millones de muestras entregadas en esas instalaciones no es trivial.
Otra forma en que los investigadores intentan llevar las pruebas a las masas es idear ensayos que puedan usarse en instalaciones de pruebas temporales, centros de pruebas de manejo e incluso en los hogares de las personas.
Al menos dos equipos están aprovechando la tecnología de edición de genes CRISPR para impulsar tales pruebas. Por ejemplo, los investigadores liderados por Zhang han desarrollado un ensayo de coronavirus que se puede ejecutar en un solo tubo de ensayo en aproximadamente una hora. Pero aún requiere calentar la muestra a aproximadamente 65°C, y no es tan sensible como un ensayo basado en PCR. «Está bien, porque es mucho más fácil de usar», dice Zhang. Cuando se probó varias veces en muestras de 12 personas infectadas con coronavirus, el ensayo detectó el virus en casi todas las ocasiones.
La prueba se basa en un enfoque que Zhang co-desarrolló en 2017, llamado SHERLOCK, que se basa en la capacidad de la maquinaria CRISPR para concentrarse en secuencias genéticas específicas. Los investigadores programan una molécula guía para engancharse a un tramo particular del genoma del SARS-CoV-2. Si la molécula guía encuentra una coincidencia, una enzima CRISPR genera una señal que puede detectarse como un brillo fluorescente o como una banda oscura en una varilla de medición de papel. El 6 de mayo, la Administración de Drogas y Alimentos de los Estados Unidos (FDA) autorizó un ensayo de coronavirus SHERLOCK para uso de emergencia. La prueba es realizada por la firma de biotecnología Sherlock BioSciences en Cambridge, Massachusetts (de la cual Zhang es cofundador), y la compañía se ha asociado con un fabricante para producir en masa los kits.
Mammoth Biosciences, una compañía de diagnóstico cofundada por la pionera CRISPR Jennifer Doudna de la Universidad de California, Berkeley, también está buscando una autorización de uso de emergencia para su prueba de coronavirus basada en CRISPR, dice la directora de tecnología y cofundadora de Mammoth, Janice Chen. La prueba se basa en un resultado anterior que muestra que la tecnología puede detectar el virus del papiloma humano. La compañía, con sede en San Francisco, California, ahora está tratando de hacer que la prueba sea lo suficientemente simple y barata para que cualquiera pueda usarla en su hogar, dice Chen. «El objetivo final es llevar los diagnósticos directamente a los consumidores: el PCR no ha podido llegar allí», dice.
Guozhen Liu, un bioingeniero de la Universidad de Nueva Gales del Sur en Sydney, Australia, dice que tecnologías como CRISPR podrían ser «un cambio reglas de juego» en la pandemia actual. Gracias a su capacidad para identificar fragmentos genéticos de forma rápida y precisa, estos enfoques «pueden encontrar una aguja en un pajar», dice Liu. Utilizan diferentes reactivos de los ensayos basados en RT-PCR, útiles cuando hay escasez de suministros químicos para pruebas estándar, y pueden diseñarse para atacar a cualquier patógeno. Por ejemplo, un equipo dirigido por el biólogo computacional Pardis Sabeti en el Broad Institute creó ‘chips’ de goma del tamaño de un teléfono inteligente que puede buscar 1,000 muestras para un solo virus, o 5 muestras para un panel de 169 virus que se sabe que infectan humanos.
Cribado de superficie
Un enfoque diferente para pruebas de diagnóstico más rápidas y baratas sería buscar moléculas que se asientan en la superficie del virus, en lugar de tratar de detectar el genoma del virus. Dicha prueba contendría un anticuerpo diseñado para unirse a una proteína específica o antígeno, similar a la tecnología que permite las pruebas de embarazo en el hogar. Estos ensayos, que son económicos de producir y simples de realizar, ya se utilizan para detectar infecciones de influenza. Pero las pruebas de antígeno no contienen un paso de amplificación de la misma manera que las pruebas de material viral, por lo que son menos sensibles.
El 8 de mayo, la FDA otorgó su primera autorización de uso de emergencia para una prueba de antígeno de coronavirus que se dirige a la proteína nucleocápside en la superficie del virus. La FDA de Taiwán está evaluando un ensayo similar que podría proporcionar resultados en 20 minutos, dice el biólogo computacional An-Suei Yang de la Academia Sinica en Taipei, quien desarrolló la prueba. El equipo de Yang usó inteligencia artificial para identificar anticuerpos que podrían unirse a proteínas en la superficie del coronavirus. Yang dice que los investigadores aún no lo han probado en muestras de coronavirus de personas infectadas.
Incluso una vez que una prueba está funcionando maravillosamente en el laboratorio, aún enfrenta un arduo viaje hacia el uso masivo. El primer desafío es verificar el rendimiento, porque la calidad puede variar. «Es un salvaje oeste para el desarrollo de ensayos», dice Catharina Boehme, directora ejecutiva de la Foundation for Innovative New Diagnostics (FIND), un grupo sin fines de lucro en Ginebra que está colaborando con la Organización Mundial de la Salud y los Hospitales Universitarios de Ginebra y que evaluará cientos de opciones de prueba de SARS-CoV-2. La mayoría de las pruebas basadas en RT-PCR que FIND ha evaluado funcionan tan bien como el estándar de oro, mientras que las pruebas de antígeno hasta ahora han estado por debajo de las expectativas, dice Boehme.
Otro obstáculo es ampliar los ensayos para la producción en masa. Dada esta restricción, Boehme cree que no es realista que todas las nuevas pruebas se implementen antes de fin de año, aunque podría ser que un pequeño número sí. Pero una vez que estén disponibles, podrían trabajar junto con el estándar de oro para acercar a los países al objetivo de millones de pruebas por semana, y preparar al mundo para la próxima pandemia.
Incluso durante esta pantemia, dice Boehme, los investigadores no deben descuidar el desarrollo de pruebas para otros virus que causan síntomas respiratorios, y monitorear condiciones como la diabetes, que pueden empeorar las perspectivas para las personas con COVID-19. «Tenemos que ir más allá de las pruebas solo para el coronavirus», dice ella.
El desarrollo de nuevas pruebas de coronavirus que podrían ayudar a poner fin a la pandemia

COVID-19 y tracto gastrointestinal: una relación más importante de lo que parece
El brote de enfermedad por coronavirus 2019 (COVID-19), causada por el virus respiratorio SARS-CoV-2, se extendió rápidamente desde China a casi todo el planeta.
Mientras que las formas de presentación típicas de esta infección, como fiebre, tos, mialgia, fatiga y neumonía, son bien reconocidas, estudios realizados de forma temprana informaron baja incidencia de síntomas gastrointestinales (GI), tales como diarrea en el rango de 1% –3.8%. Otro estudio mostró una mayor tasa de síntomas gastrointestinales con diarrea y náuseas 10.1% y vómitos en 3.6%.
Varios artículos informan sobre síntomas gastrointestinales, detección del virus en las heces y posibles aspectos fisiopatológicos, incluyendo la expresión del receptor viral en el tracto gastrointestinal. Dos grandes estudios clínicos realizados en China se centraron en los síntomas gastrointestinales y en la detección del virus en las heces. Jin et al investigó a 74 pacientes infectados con SARS-CoV-2 con síntomas gastrointestinales como diarrea, náuseas y vómitos. Hasta un 28% de aquellos pacientes con síntomas gastrointestinales no tenían síntomas respiratorios. Mostraron que este grupo de pacientes en comparación con pacientes sin síntomas gastrointestinales (n = 577) tuvo en general una enfermedad más grave/crítica, más pacientes con fiebre >38.5 ° C, y tasas más altas de daño hepático según lo evaluado por el aumento de los niveles de las transaminasas.
Entre el total de pacientes estudiados infectados por el SARS-CoV-2 (n = 651) el 11.4% experimentó síntomas gastrointestinales, lo que representa un porcentaje más alto que los reportados en anteriores estudios. En otro estudio, Lin et al investigaron 95 paciente con infección por SARS-CoV-2 con especial énfasis en los síntomas gastrointestinales.
En general, 58/95 casos (61,1%) mostraron evidencia de síntomas gastrointestinales con diarrea (24,2%), náuseas (17,9%), vómitos (4,2%) e insuficiencia hepática según lo evaluado por los niveles elevados de transaminasas (32.6%). Realizaron endoscopia en seis pacientes demostrando que SARS-CoV-2 podía ser detectado en varios lugares del tracto GI en tres de los seis sujetos a los cuales se realizó biopsia durante la endoscopía. En dos pacientes graves, el virus pudo detectarse en esófago, estómago, duodeno y recto lo que demuestra que este virus está presente en todo el tracto gastrointestinal. Finalmente fueron capaces de detectar el virus en 52.4% (n = 22) de muestras fecales evaluadas. Por lo tanto, ambos estudios destacan la prevalencia de síntomas gastrointestinales en la enfermedad COVID-19. En el primer caso de infección por SARS-CoV- 2 reportado desde los Estados Unidos, el virus también fue observado en las heces el día 7 de la enfermedad.
Xiao et al investigaron 73 pacientes infectados por SARS-CoV- 2 hospitalizados en China y el 53,4% de los pacientes resultó positivo a la presencia de virus en las heces desde el día 1 al 12 de infección. Es importante destacar que en este estudio más del 20% de los pacientes infectados tuvieron resultados positivos de virus en las heces incluso después de la eliminación del virus del tracto respiratorio. Resultados similares provenientes de Singapur mostraron que el 50% de los pacientes con COVID-19 tenían el virus detectable en las heces, pero sólo aproximadamente la mitad de estos pacientes presentaron síntomas digestivos. Por lo tanto, la evidencia en cuanto a los síntomas gastrointestinales y la detección del virus en las heces en la mayor parte de los sujetos infectados va en aumento, aunque no parece existir una correlación clara entre los síntomas gastrointestinales y la carga viral detectable en las heces.
Queda menos claro por qué y cómo SARS-CoV- 2 induce síntomas gastrointestinales, y en segundo término, si SARS-CoV-2 puede ser transmitido a través del tracto gastrointestinal.
Un pre-requisito para la infección por coronavirus es su entrada en las células huésped. De manera similar a su congénere SARS-CoV, SARS-CoV- 2 utiliza la enzima conversora de angiotensina -2 (ACE2) como receptor viral para ingresar a las células huésped, y ACE2 es un importante regulador de la inflamación intestinal.
Liang et al. examinaron la expresión y distribución de ACE2 en tejidos humanos y en diferentes poblaciones celulares. Mediante el análisis de la secuencia de ARN encontraron que ACE2 se expresa en forma importante en el intestino delgado, especialmente en los enterocitos proximales y distales. También encontraron otros dos receptores de entrada viral para humanos del coronavirus 229E y del virus causante del síndrome respiratorio de medio oriente, los cuales fueron altamente expresados en enterocitos. Para tomar estos hallazgos adicionales, Zhang et al examinaron la expresión de ACE2 en la composición celular de pulmón, esófago, estomago, íleon y colon.
Encontraron que la entrada exitosa del virus de SARS-CoV- 2 depende no sólo de la presencia del receptor celular ACE2 sino también la serina proteasa celular transmembrana 2 (TMPRSS2), que escinde la proteína S del coronavirus humano en la membrana celular. Ambas proteínas son críticas para la fusión de virus y las membranas celulares. ACE2 y TMPRSS2 no sólo se co-expresaron en células alveolares pulmonares tipo 2, esofágicas y gástricas, sino también en el íleon y colon, lo que sugiere que el virus puede invadir enterocitos del tracto digestivo. En el esófago, ACE2 se expresó significativamente en las células epiteliales superiores y estratificadas, y este hallazgo puede explicar la detección de SARS-CoV- 2 en la erosión esofágica. Un hallazgo intrigante fue una expresión cuantitativamente más alta de ACE2 en enterocitos absorbentes del íleon y el colon que en el pulmón. No está claro si la inflamación intestinal exacerba la expresión de ACE2 en el intestino y ejerce un mayor riesgo para los pacientes con enfermedad inflamatoria intestinal. En relación a este problema se informó la muerte en un paciente anciano con colitis ulcerativa aguda severa que fue tratada con dosis altas de corticosteroides intravenosos y posteriormente desarrolló neumonía por COVID-19.
En aproximadamente el 50% de los casos de COVID-19, la presencia de SARS-CoV- 2 en muestras de heces evidenció la presencia de SARS-CoV-2 en la mucosa intestinal de pacientes infectados lo que sugiere que los síntomas entéricos podrían ser causados por la invasión de ACE2 expresado en los enterocitos.
En más de la mitad de los pacientes, las muestras fecales permanecieron positivas para SARS-CoV2 durante un promedio de 11 días después de la desaparición del virus en las vías respiratorias.
Un estudio reciente adicional confirmó que 8 de cada 10 niños infectados tenía hisopos rectales virales persistentemente positivos después de que la prueba nasofaríngea fue negativa.
Es importante destacar que el SARS-CoV- 2 fue detectado en microscopía electrónica en las heces de dos pacientes que no presentaron como síntoma diarrea, destacando la potencial transmisión fecal-oral.
En conclusión, estos estudios proporcionan nuevos conocimientos sobre nuestra comprensión de la prevalencia, etiología y potencial mecanismos de infección del COVID-19 en el tracto gastrointestinal lo cual es crucial para definir medidas de prevención, atención clínica y estrategias de tratamiento.
Permanecen preguntas y desafíos sin respuesta, tal como la importancia de la detección del virus en las heces e hisopados rectales positivos de sujetos asintomáticos, el rol de ACE2 como mediadora directa para el ingreso de SARS-CoV-2 en el tracto gastrointestinal y cómo el virus podría sobrevivir al paso por el ambiente de pH extremo del aparato digestivo.
Actualmente, la permanecía viral a nivel fecal de forma prolongada en pacientes infectados, incluso después del aclaramiento viral en el tracto respiratorio sugiere que la prueba de heces debe considerarse en pacientes con COVID-19 como medida de prevención ante la posible transmisión de pacientes hospitalizados.
Se requiere investigación adicional para determinar la viabilidad e infectividad de SARS-CoV- 2 en las heces para controlar la propagación del virus, especialmente en portadores asintomáticos.
COVID-19 y tracto gastrointestinal más de lo que parece
Vacuna COVID-19: Moderna va por la última fase de prueba
La empresa estadounidense Moderna comenzará la fase 3, última etapa experimental de su vacuna contra el SARS-CoV-2, el 27 de julio.
En dicha etapa participarán 30.000 personas en 87 sitios diferentes de Estados Unidos. El objetivo es comprobar que la vacuna sea segura y eficaz para evitar el contagio de la infección.
La diferencia del prototipo de vacuna conocida como ARNm-1273 está en que está basada en la plataforma de material genético llamado ARN mensajero para hacer que las células produzcan la proteína espiga del coronavirus. De acuerdo con el protocolo del estudio, se inyectarán dos dosis, con un mes de diferencia.
En el anterior estudio de fase II, se encontró que la primera dosis administrada derivó en la generación de anticuerpos, mientras que la segunda dosis produjo una respuesta inmune significativa.
El pasado 14 julio la compañía estadounidense informó que la vacuna produjo anticuerpos suficientes para neutralizar la enfermedad en los pacientes que recibieron la dosis. Estos resultados se dieron a conocer en el New England Journal of Medicine, en el cual se especifica que el estudio fue realizado en 45 voluntarios e iniciado en el mes de marzo.
Los expertos informaron que las personas que recibieron las dosis desarrollaron una cantidad comparable de anticuerpos neutralizantes a la que se observa en personas convalecientes, los cuales son claves para bloquear la infección.
L.A. Jackson et al. en su informe preliminar publicado en New England Journal of Medicine concluye que la vacuna mRNA-1273 indujo respuestas inmunitarias anti-SARS-CoV-2 en todos los participantes, no identificándose problemas de seguridad limitantes en los ensayos.
La compañía con sede en Cambridge, Massachusetts, informó el mes pasado que tendría la capacidad de manufacturar entre 500 y 1.000 millones de dosis al año a partir de 2021, en colaboración con la farmacéutica suiza Lonza.
Información disponible en:
https://www.nejm.org/doi/pdf/10.1056/NEJMoa2022483
https://www.infobae.com/america/mexico/2020/07/19/vacuna-contra-covid-19-moderna-va-por-ultima-fase-de-prueba/
Vacuna COVID 19

Compromiso hepático en COVID-19: revisión sistemática y metaanálisis
El impacto de COVID-19 en el hígado aún no ha sido investigado. La mayor parte de los estudios atribuyen la gravedad de esta enfermedad a sus complicaciones respiratorias.
Dipesh Kumar Yadav y colaboradores realizaron un metaanálisis para estimar el pronóstico de los pacientes con COVID-19 estratificados según la lesión hepática.(1) Incluyó nueve estudios con un total de 2115 pacientes.
Los estudios publicados sobre COVID-19 han demostrado que un 37,2% a 76,3% de los pacientes tienen anormalidades en la función hepática. Además, los pacientes con COVID-19 con enfermedad hepática crónica (CLD, chronic liver disease) podrían desarrollar descompensaciones hepáticas como resultado de una respuesta inflamatoria sistémica inducida por COVID-19. Los autores encontraron que la prevalencia de CLD fue del 4% entre los pacientes con COVID-19, siendo cirrosis y hepatitis B las más comunes. Del mismo modo, la incidencia de lesión hepática fue del 27%. Cabe destacar que los pacientes mayores con COVID-19 tenían un mayor riesgo de lesión hepática.

Ilustración 1: Forest plot con prevalencia de lesión hepática en pacientes con COVID-19.(1)
La función hepática anormal en estos pacientes es posiblemente multifactorial: lesión hepática inducida por fármacos (DILI, drug-induced liver injury), repercusión del SARS-CoV-2 en el hígado e inflamación cruzada en cuadros agudos. En general, 7.14% –64.15% de los pacientes con COVID-19 aumentaron los niveles de aspartato-aminotransferasa (AST), alanina-aminotransferasa (ALT), gamma-glutamiltransferasa (GGT) y bilirrubina total.
La mayoría de los pacientes con COVID-19 tuvieron una reducción notable en los recuentos de CD4 y CD8. Los pacientes graves mostraron un aumento en los marcadores inflamatorios, como interleucina-6, velocidad de sedimentación globular (ESR, erythrocyte sedimentation rate), dímero D, ferritina, recuentos de neutrófilos y proteína C reactiva (PCR), lo que sugiere una «tormenta de citoquinas«.
Al mismo tiempo, el metaanálisis mostró un recuento absoluto de linfocitos significativamente menor y una velocidad de sedimentación globular más alta en el grupo con lesión hepática, en comparación con el grupo sin lesión hepática. Sin embargo, no se observaron diferencias notables en el PCR y en el recuento absoluto de neutrófilos entre los dos grupos.
La lesión hepática inducida por fármacos (DILI) no debe pasarse por alto en pacientes con COVID-19. Cai y colaboradores encontraron que el uso de lopinavir/ritonavir se asoció con la lesión hepática de manera estadísticamente significativa. (2) Sin embargo, Fan et al no encontraron ninguna diferencia en la prevalencia de lesión hepática entre pacientes con y sin la administración de estos medicamentos. (3) El metaanalisis de Dipesh Kumar Yadav y colaboradores (1) encontró que el grupo con lesión hepática tuvo una administración considerablemente mayor de lopinavir/ritonavir que el grupo sin daño hepático (OR: 4,15; IC del 95%: 2,36 a 7,29, p <0,00001). No se observó diferencia estadísticamente significativa con otros medicamentos.
A su vez, los pacientes con COVID-19 y daño hepático, tuvieron una enfermedad más grave (OR: 2.57, IC 95% 1.25 a 5.26, p = 0.01) y una mayor mortalidad (OR: 1.66, IC 95%: 1.04 a 2.64, p = 0.03) (Ver Ilustración 2). Sin embargo, la duración de la estadía hospitalaria no fue significativamente diferente entre los grupos. La tasa de severidad y mortalidad en pacientes con COVID-19 y daño hepático fue 53,5% y 23,5%, respectivamente.

Ilustración 2: Forest plot sobre el pronóstico de pacientes con COVID-19 con daño hepático (1)
Referencia:
1. Yadav DK, Singh A, Zhang Q, et al. Involvement of liver in COVID-19: systematic review and meta-analysis. Gut Published Online First: 15 July 2020.
doi:10.1136/gutjnl-2020-322072
2. Cai Q, Huang D, Yu H, et al. COVID-19: abnormal liver function tests. J Hepatol 2020;S0168-8278
3. Fan Z, Chen L, Li J, et al. Clinical features of COVID-19-Related liver functional abnormal-ity. Clin Gastroenterol Hepatol 2020;18:1561–6.
Secuelas hepáticas
Los residentes más jóvenes del condado de Los Ángeles se están contagiando cada vez más COVID-19
El aumento de la infección por coronavirus en el condado de Los Ángeles sigue siendo impulsado por personas más jóvenes, con la mayoría de los infectados menores de 41 años.
Las autoridades dijeron el domingo que el 53% de los 2,848 casos nuevos reportados para el día ocurrieron entre ese grupo. En general, el 52% de los casos hasta la fecha en el condado han sido personas menores de 41 años. En todo el estado, las personas de 18 a 34 años representan el mayor porcentaje de casos confirmados de coronavirus, seguidos de los 35 a 49, según el rastreador de coronavirus de The Times.
El aumento de los casos comenzó en junio cuando se reabrieron partes de la economía. Las autoridades creen que el coronavirus está afectando a las personas más jóvenes que retomaron la vida social del verano o que reanudaron el trabajo. Los que mueren por COVID-19 continúan siendo personas mayores de 80 años siendo el grupo más grande, seguidos por los de 65 a 79.
Ha habido una creciente preocupación por el aumento de jóvenes californianos que contraen COVID-19. Este mes, el gobernador Gavin Newsom los llamó «los jóvenes invencibles», que creen que no corren el riesgo de enfermarse o transmitir el virus a otros.
«Son invencibles, pero no sienten que les va a afectar, y si lo hace, no es una gran carga», dijo.
Con las hospitalizaciones alcanzando nuevos máximos este mes, los funcionarios han cerrado algunos negocios, incluidos bares, restaurantes interiores, centros comerciales y otros minoristas. Sigue habiendo debate sobre si California reabrió demasiado pronto.
El alcalde de Los Ángeles, Eric Garcetti, dijo el domingo que Los Ángeles abrió demasiado rápido y nuevamente advirtió que la ciudad estaba cerca de imponer algún tipo de nueva orden de quedarse en casa si las condiciones no mejoran.
Se le preguntó a Garcetti en CNN sobre un editorial del Times que criticaba la rápida reapertura de California, seguido de un aumento importante tanto en los nuevos casos de COVID-19 como en las hospitalizaciones. «Creo que mucha gente no entiende, los alcaldes a menudo no tienen control de lo que se abre y no lo hace, eso es a nivel estatal o de condado», dijo Garcetti. «Y estoy de acuerdo en que esas cosas sucedieron demasiado rápido».
A pesar de sus comentarios, a los líderes locales como Garcetti se les permite emitir órdenes de cierre y restricción domiciliaria que son más estrictas que las emitidas por el condado o el estado, pero no reglas que son más indulgentes, dijeron las autoridades.
El alcalde ha sugerido previamente que él estará a cargo de decidir cuándo debe reabrir la ciudad. «Nuestro momento de apertura puede ser distinto al de otras partes del estado», dijo a principios de mayo. «Reabriré nuestra ciudad con cuidadosa consideración, guiado por profesionales de la salud pública».
Garcetti también dijo el domingo que la ciudad estaba «al borde» de las nuevas restricciones, pero no dio más detalles. El alcalde ha hecho el comentario antes en las últimas dos semanas, diciendo que la ciudad actuaría si los casos continuaban aumentando, incluso después de una serie de restricciones impuestas por el estado este mes que incluyeron la prohibición de comer en restaurantes interiores y el cierre de bares, centros comerciales y otros minoristas en el condado de Los Ángeles y muchos otros.
El alcalde instó a la paciencia, diciendo que tomará hasta tres semanas saber si los cierres han ayudado a frenar la propagación del coronavirus.
Funcionarios de salud pública del condado de Los Ángeles informaron 2.848 nuevos casos de coronavirus el domingo.
Hay 2.216 personas hospitalizadas con el virus, informó el departamento de salud del condado. El domingo fue el quinto día consecutivo en que el número de hospitalizaciones superó las 2.100 y la primera vez que las hospitalizaciones superaron las 2.200.
Entre los hospitalizados, el 26% está en unidades de cuidados intensivos y el 19% está conectado a ventiladores. El último informe también incluye 11 muertes, lo que eleva el total del condado a 4.095.
«Continuamos alcanzando hitos preocupantes y hoy estamos viendo el mayor número de hospitalizaciones por COVID-19», dijo la directora de salud pública del condado de L.A., Barbara Ferrer, en un comunicado. “En este momento, los adultos jóvenes están siendo hospitalizados a un ritmo nunca antes visto. No importa cuán joven seas, eres vulnerable a este virus. Insto a todos a asumir la responsabilidad colectiva: mantenerse físicamente separados de las personas con las que no conviven, usar una máscara adecuada cuando estén fuera de su hogar, y permanecer en sus casas tanto como sea posible «.
Ver Nota
Los Angeles Times
Los residentes más jóvenes del condado de Los Ángeles se

Resultados clínicos preliminares de la vacuna candidata BNT162b1 desarrollada por BioNTech y Pfizer
Desde comienzos de 2020 se ha comenzado una búsqueda exhaustiva de una vacuna contra el virus SARS-CoV-2, lo cual es esencial generar inmunidad contra este virus y detener el impacto socioeconómico ocasionado por esta pandemia.
La compañía BioNTech, asociada con Pfizer, ha desarrollado un programa llamado BNT162 dentro del cual se desarrollaron cuatro vacunas candidatas basadas en ARN mensajero. BNT162b1 y BNT162b2 son las vacunas candidatas más promisorias y consisten en secuencias de ARN mensajero dispuesto en el interior de nanopartículas lipídicas. En particular, la vacuna BNT162b1 codifica el dominio de receptor de unión (RBD) de la proteína espiga de SARS-CoV-2 modificado; ya que cuenta con la adición de un dominio de trimerización (dominio C-terminal de fibritin, proteína del bacteriófago T4), para aumentar la inmunogenicidad.
El estudio clínico de fase 1 – 2 realizado para analizar las vacunas candidatas de BNT162, ya ha mostrado resultados preliminares sobre BNT162b1, que serán publicados próximamente. Si bien este estudio aún sigue en curso en Estados Unidos y Alemania, se han obtenido resultados del ensayo en Estados Unidos, y se espera que en el correr del mes de julio también se presenten resultados preliminares en Alemania. Este ensayo se trata de un estudio de seguridad, tolerabilidad e inmunogenicidad en 45 voluntarios sanos entre 18-55 años de edad, randomizado, controlado por placebo, donde el observador estaba cegado. El diseño contó con dosis escaladas de 10, 30 o 100 ug de BNT162b1, donde cada participante recibió dos dosis separadas entre sí por 21 días. Se evaluaron los resultados obtenidos hasta el día 14 después de la segunda dosis.
En los 7 días posteriores a cada inyección se observó que las reacciones adversas reportadas eran en su mayoría en el sitio de inyección, y que eran crecientes a dosis mayores. Los participantes que recibieron placebo también experimentaron esta reacción adversa en un 22% de los casos. Todas las reacciones locales fueron leves o moderadas, excepto por un reporte que se correspondió con dolor severo posterior a la primera dosis de 100ug de la vacuna. Las reacciones adversas sistémicas más frecuentes en grupos de tratamiento y placebo fueron fatiga y dolor de cabeza, las cuales fueron reportadas en los 7 días subsiguientes a la administración. Adicionalmente, se reportaron escalofríos, fiebre, dolor muscular y dolor en articulaciones en los pacientes que recibieron la vacuna candidata. Los eventos adversos sistémicos fueron proporcionales a la dosis y en particular luego de la segunda dosis. La fiebre se resolvió dentro de 24 horas. Se reportaron eventos adversos en el 50% de los participantes que recibieron las dosis de 10 y 30ug, en el 58% de los que recibieron la dosis de 100ug, y en el 11% de los que recibieron placebo. Se observó en algunos pacientes una disminución en el conteo de linfocitos después de la primera dosis (grado 1 y grado 3), que fueron transitorias y volvieron a valores normales a los 6-8 días después de la administración. Se observó neutropenia de grado 2 en 2 pacientes luego de la segunda dosis, los cuales están actualmente en seguimiento y hasta la fecha no han manifestado eventos adversos o manifestaciones clínicas desencadenadas por la neutropenia. No se reportaron eventos adversos serios y no hubo anormalidades post-vacunación.
La inmunogenicidad fue analizada mediante la evaluación de la concentración de IgG de unión al dominio RDB de la proteína espiga y los títulos de anticuerpos neutralizantes de SARS-CoV-2, en los días 0,7, 21, 28 y 35. Se observaron niveles de IgG anti-RBD de 534-1778 U/mL luego de 21 días, mientras que en el suero de 38 pacientes convalecientes de SARS-CoV-2 los niveles luego de 14 días fueron en promedio 602 U/mL. Luego de la segunda dosis de 10 y 30 ug, el valor de IgG anti-RBD fue de 4813-27872 U/mL. Las concentraciones de IgG anti-RBD no aumentaron más allá de 21 días después de la primera vacunación en los participantes que recibieron una dosis de 100ug de BNT162b1. En los participantes que recibieron las dosis de 10 y 30ug, se observaron niveles altos de IgG anti-RBD hasta la última evaluación (día 35, 14 días después de la segunda dosis). Estas concentraciones fueron de 5.880-16.166 U/mL, más elevadas que las observadas en el suero de pacientes convalecientes (602 U/mL).
Para todas las dosis se observaron modestos aumentos de los niveles de neutralización del SARS-CoV-2, 21 días después de la primera dosis. Se lograron niveles neutralizantes sustancialmente mayores 7 días después de la segunda dosis de 10 o 30 µg, llegando a 168-267 U/mL, en comparación con 94 U/mL para el suero humano convaleciente. La cinética y la durabilidad de los niveles de neutralización están siendo monitoreadas.
Los autores destacan que “estos hallazgos clínicos para la vacuna candidata BNT162b1 son alentadores y apoyan firmemente el desarrollo clínico acelerado y la fabricación “en riesgo” para maximizar la oportunidad de producir rápidamente una vacuna contra el SARS-CoV-2, con el fin de prevenir la enfermedad COVID-19”.
Debido a estos resultados preliminares, la FDA otorgó la vía rápida de evaluación para las vacunas candidatas mencionadas. El proceso de vía rápida facilita el desarrollo y la revisión de nuevos fármacos y vacunas que quieren tratar o prevenir condiciones serias. Özlem Türeci, Director Médico de BioNTech comentó: «Nos complace haber recibido la designación de vía rápida de la FDA para dos de nuestras vacunas candidatas y esperamos trabajar estrechamente con la FDA, junto con nuestro socio Pfizer, para acelerar el desarrollo clínico».
Por otra parte, Peter Honig, Vicepresidente de Asuntos Regulatorios Mundiales de Pfizer ha expresado que «La decisión de la FDA de otorgar a estos dos candidatos la designación de vía rápida significa un hito importante en los esfuerzos por desarrollar una vacuna segura y eficaz contra el SARS-CoV-2». «Esperamos seguir trabajando estrechamente con la FDA a lo largo del desarrollo clínico de este programa, el Proyecto Warp Speed, para evaluar la seguridad y la eficacia de estas vacunas candidatas».
Si bien el estudio cuenta con limitaciones (bajo número de participantes, empleo de suero humano convaleciente como comparador, falta de seguimiento posterior a los 35 días), muestra resultados prometedores sobre una primera vacuna contra el SARSCoV2. Se requieren más resultados de estudios clínicos sucesivos para brindarle robustez a los resultados preliminares, y confirmar los hallazgos obtenidos. Ambas compañías esperan iniciar el estudio clínico de fase 2b-3 (con 30.000 participantes) a finales de julio. Si los estudios en curso tienen éxito y las vacunas candidatas reciben la aprobación de las autoridades reguladoras, ambas compañías esperan producir hasta 100 millones de dosis para finales de 2020, y proyectan una producción de más de 1.200 millones de dosis para finales de 2021.
Más información
– Mulligan et al. Phase 1/2 Study to Describe the Safety and Immunogenicity of a COVID-19 RNA Vaccine Candidate (BNT162b1) in Adults 18 to 55 Years of Age: Interim Report. medRxiv. 2020. Doi:
https://doi.org/10.1101/2020.06.30.20142570
– A Trial Investigating the Safety and Effects of Four BNT162 Vaccines Against COVID-2019 in Healthy Adults. Clinical Trials. 2020. Extraído de:
https://clinicaltrials.gov/ct2/show/NCT04380701
– Pfizer and BioNTech Granted FDA Fast Track Designation for Two Investigational mRNA-based Vaccine Candidates Against SARS-CoV-2. BIONTECH. 2020. Extraído de:
https://biontechse.gcs-web.com/news-releases/news-release-details/pfizer-and-biontech-granted-fda-fast-track-designation-two
Resultados clínicos preliminares de la vacuna candidata BNT162b1 desarrollada por BioNTech y Pfizer

Vacunación BCG: ¿tiene un impacto en la pandemia de COVID-19?
Los datos disponibles sobre COVID-19 han revelado que la incidencia y la mortalidad de la enfermedad varían entre los países. La variabilidad podría deberse a una variedad de factores, tales como el origen étnico, los hábitos alimenticios, el clima, las actividades sociales, las diferencias genéticas y las estructuras de gobierno. Un factor potencial que podría desempeñar un papel central, tanto en la susceptibilidad a la infección como en su gravedad, es la vacunación contra la tuberculosis (Bacillus Calmette – Guerin, BCG).
Vacunación BCG y COVID-19
La cepa de Mycobacterium bovis BCG se desarrolló en 1921 en el Instituto Pasteur a través de la atenuación mediante pasajes seriados de una cepa de M. bovis, aislada de una vaca con mastitis tuberculosa. Actualmente, alrededor de 100 millones de niños se vacunan cada año en todo el mundo. Sin embargo, la vacuna exhibe poca eficacia contra la tuberculosis pulmonar adulta y, por lo tanto, varios países han descontinuado la inmunización con BCG. Posteriormente se demostró que BCG exhibe efectos protectores contra la lepra, la úlcera de buruli y otras enfermedades, incluidas aquellas no asociadas con micobacterias. BCG es un potente inmunomodulador, empleándose inclusive para el tratamiento de cánceres como el de la vejiga. (2)
Para investigar el impacto de la vacuna BCG en la propagación de COVID-19, Sharma, A. y colaboradores publicaron el 08 de julio del 2020 en la revista The Nature (1) un análisis de los datos de la enfermedad y la vacunación. Clasificaron los países en tres grupos siguiendo los datos obtenidos de BCG Atlas («The BCG World Atlas» http://www.bcgatlas.org/index.php):
i. Países que nunca adoptaron un programa nacional de vacunación con BCG
ii. Países que tenían un programa de vacunación masiva con BCG pero lo descontinuaron
iii. Países con una política nacional activa de vacunación con BCG.
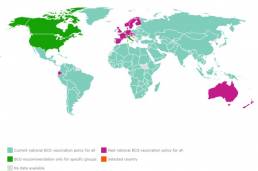
Figura extraída de http://www.bcgatlas.org/index.php
Luego, obtuvieron los datos de incidencia y mortalidad de COVID-19 del sitio web www.worldometer.info. Estimaron el número de casos por millón por habitante y presentaron las medidas normalizadas para la incidencia y mortalidad. Los resultados muestran que los países sin una política universal de BCG (como Bélgica, Italia, los Estados Unidos y los Países Bajos) tienen una mayor incidencia de COVID-19 (2810.9 ± 497.1 por millón de habitantes) en comparación con países con una política nacional de BCG en curso (570,9 ± 155,6 por millón de habitantes). La incidencia para los países que descontinuaron la vacuna BCG fue intermedia entre estos dos grupos (1844.67 ± 508.89 por millón de habitantes (Ilustración 1a).
A su vez, los países con una política universal de BCG exhibieron la menor cantidad de muertes debido a COVID-19 (92.4 ± 34.7 por millón de habitantes), significativamente menor que la de los países que descontinuaron la vacunación universal con BCG (104.5 ± 33.6 por millón de habitantes). Los países sin vacunación BCG fueron los más afectados (186,1 ± 56,8 por millón de habitantes). (Ilustración 1b)
Este tipo de análisis no refleja el verdadero impacto de BCG contra COVID-19, ya que un país con un mayor porcentaje de población en edad avanzada puede informar más muertes que un país con una población más joven, debido al aumento de comorbilidades que empeoran la gravedad de la enfermedad. Desafortunadamente, no hay suficientes datos públicos disponibles para analizar el impacto de tales factores de confusión. Por lo tanto, los autores investigaron cómo la incidencia y la mortalidad varía entre los diferentes grupos de edad en una población. Consideraron cinco grupos de edad diferentes: <15, 15–44, 45–64, 64–79 y mayores de 80 años. Los resultados indican que el número de infectados en todos los grupos de edad siempre es mayor para los países sin una política de vacunación universal BCG. Además, las diferencias entre los países con una política universal de vacuna BCG y los países sin dicha política aumentan con la edad, y alcanzan su punto máximo para los grupos de edad de 45-64 y 65-79 años (Ilustración 1b y 1c). La diferencia en el número de casos confirmados en estos grupos de edad es de 550–600 por millón de habitantes entre países con política de vacunación, vs sin política de vacunación universal BCG. Esto sugiere una correlación inversa entre la vacuna BCG y COVID-19 en todos los grupos de edad.
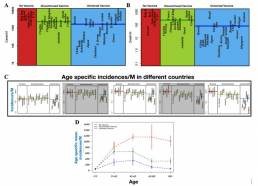
Ilustración 1: a) y b) representan incidencia y mortalidad por millón de habitantes en todos los países que emplean la vacunación universal continua; los que han descontinuado la vacunación; y los que nunca adoptaron la vacuna BCG. c) muestra la incidencia por millón de habitantes por grupo de edad para estos tres tipos de países. d) muestra el número medio específico de casos de incidentes por millón de habitantes por edad para diferentes tipos de países.(1)
Los autores estudiaron también la asociación entre la vacunación con BCG y la mortalidad con COVID-19 para diferentes grupos de edad. Los resultados muestran que la distribución de casos fatales por millón de habitantes en diferentes grupos de edad para países sin vacunación masiva y países con vacunación descontinuada no es significativamente diferente (p = 0,41, prueba U de Mann-Whitney)

Ilustración 2: a) Muertes por millón de habitantes por grupo de edad para países que emplean la vacunación BCG universal continua; los que han descontinuado la vacuna; y los que nunca adoptaron. b) Número promedio de muertes por millón por grupo de edad para diferentes tipos de países. (1)
A su vez, evaluaron la relación entre la incidencia y mortalidad de COVID-19 y la vacunación BCG, para varias cepas de BCG atenuadas (Ilustración 3). Hallaron que los países que adoptan una mezcla de diferentes cepas de la vacuna BCG, como Corea del Sur y Filipinas, informaron un menor número de casos confirmados y fatales. Las cepas BCG-Dinamarca y BCG-Rusia se correlacionaron pobremente en términos de limitar la propagación de COVID-19. Brasil, siendo un país con una política universal de vacunación BCG, tuvo el número de muertes por COVID-19 más alto entre los países con una estrategia de vacunación similar. Esto podría deberse al uso de la cepa BCG-Brasil, ineficaz contra COVID-19.
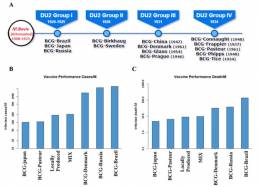
Ilustración 3: a) Tipos de cepas de BCG. b) Número de casos con COVID19 confirmado. c muertes observados para diversas cepas de BCG.
Estos datos sugieren que la vacuna BCG se correlaciona con una menor incidencia y gravedad de la enfermedad COVID-19 en diferentes países. Muy recientemente varios países, incluidos Estados Unidos, Australia, Alemania y los Países Bajos, han iniciado un proyecto de vacunación con BCG con el objetivo de controlar el COVID. (3,4)
Referencias:
1. Sharma, A., Kumar Sharma, S., Shi, Y. et al. BCG vaccination policy and preventive chloro-quine usage: do they have an impact on COVID-19 pandemic?. Cell Death Dis 11, 516 (2020).
https://doi.org/10.1038/s41419-020-2720-9
2. Alhunaidi, O. & Zlotta, A. R. The use of intravesical BCG in urothelial carcinoma of the bladder. Ecancermedicalscience13, 905 (2019).
3. Craven, J. COVID-19 vaccine tracker. Raps
https://www.raps.org/news-and-articles/news-articles/2020/3/covid-19-vaccine-tracker (2020).
4. An old TB vaccine finds new life in coronavirus trials.
https://www.the-scientist.com/news-opinion/an-old-tb-vaccine-finds-new-life-in-coronavirus-trials-67504 (2020).
Nota_BCG y COVID-19

Un medicamento contra la covid-19 podría reducir un 79% el riesgo de formas severas
Un medicamento llamado SNG001 reduciría en 79% el riesgo de desarrollar una forma severa de covid-19, según resultados preliminares publicados el lunes por el laboratorio británico que lo produce, Synairgen. Este tratamiento inhalado utiliza el interferón beta, una proteína natural que participa en la respuesta del organismo contra los virus.
El estudio de la universidad de Southampton con 101 pacientes llega a la conclusión de que quienes son tratados con este medicamento tienen un 79% menos de posibilidades de desarrollar formas severas de la enfermedad que los que recibieron un placebo. Estas formas severas obligan a usar respirador y pueden resultar mortales. Los pacientes tratados con SNG001 tienen más del doble de posibilidades de curarse en relación a los que recibieron un placebo. Tres de los pacientes (el 6%) tratados con el placebo murieron, mientras que no hubo ningún fallecido entre los que fueron tratados con SNG001.
El estudio se llevó a cabo con una muestra reducida de pacientes y no fue evaluado por un comité de lectura. Sin embargo podría revolucionar la manera como se trata el covid-19.
Según el director general de Synairgen, Richard Marsden, podría tratarse de «un gran avance».
«Los resultados confirman nuestra convicción de que el interferón beta por inhalación presenta un potencial enorme como tratamiento para restaurar la respuesta inmunitaria de los pulmones, mejorando la protección, acelerando la recuperación y combatiendo el impacto del virus SARS-CoV-2», dijo en un comunicado Tom Wilkinson, profesor de medicina en la universidad de Southampton, quuien dirige el ensayo.
Descargar comunicado aquí:
https://www.synairgen.com/wp-content/uploads/2020/07/200720-Synairgen-announces-positive-results-from-trial-of-SNG001-in-hospitalised-COVID-19-patients.pdf
Un medicamento contra la covid-19 podría reducir un 79% el riesgo de formas severas

Hallazgos imagenológicos de neumonía por COVID-19 en pacientes asintomáticos
En diciembre de 2019, se identificó primera vez un nuevo coronavirus en Wuhan, China. Actualmente denominado coronavirus tipo 2 del síndrome respiratorio agudo grave (SARS-CoV2) y anteriormente llamado 2019-nCoV. El SARS-CoV-2, causa una enfermedad respiratoria llamada Coronavirus 2019 (COVID-19) que fue nombrada oficialmente por la Organización Mundial de la Salud (OMS) el 11 de febrero de 2020. Siete meses después, a la fecha de hoy, 17 de julio de 2020, hay 13.885.746 de casos confirmados de COVID-19 a nivel mundial, con un total de 592.573 fallecimientos.
Si bien la mayoría de los pacientes infectados presentan síntomas leves, las personas portadoras del virus asintomáticas pueden llegar a ser hasta un 45%. Además de ser en una fuente de contagio de SARS-CoV2 y de jugar un papel significativo en la temprana y continua propagación de COVID-19, estos «portadores o transmisores asintomáticos» pueden progresar rápidamente, incluso presentando en la evolución un síndrome de dificultad respiratoria aguda con alta tasa de letalidad. En esta línea, la última investigación mostró que el 30% – 60% de los pacientes infectados con SARS-CoV-2 no tenían síntomas o presentaban síntomas leves, pero su capacidad para propagar el virus era alta lo que podría estar causando nuevos brotes. Por lo tanto, es esencial identificar los casos asintomáticos o sintomáticos leves para controlar la epidemia de SARS-CoV-2.
La tomografía computarizada (TC) de tórax, especialmente la TC de alta resolución (TCAR) es uno de los métodos de diagnóstico principal según el «Diagnóstico de neumonía y guía de tratamiento para la infección por SARS-CoV-2 (versión de prueba 5)» emitido por la Comisión Nacional de Salud de la República Popular de China (http://www.nhc.gov.cn/). Los hallazgos de la TC juegan un papel importante en la detección de anormalidades pulmonares, facilitando la identificación temprana de las enfermedades.
Un trabajo publicado por Meng H y colaboradores en julio de 2020, tuvo como objetivo caracterizar las imágenes de la TC y el curso clínico de los pacientes asintomáticos con neumonía por COVID-19 con el fin de comprender el desarrollo de la enfermedad en pacientes asintomáticos, así como facilitar la detección y el aislamiento de pacientes con neumonía por el nuevo coronavirus, especialmente los casos altamente sospechosos y asintomáticos con pruebas negativas de ácido nucleico (prueba de RT-PCR, retro-transcriptasa + reacción en cadena de la polimerasa, en tiempo real).
En este estudio, se incluyeron 58 pacientes asintomáticos con neumonía por COVID-19 confirmados por RT-PCR para SARS-CoV-2 en el Hospital Renmin de la Universidad de Wuhan, China, entre el 1 de enero de 2020 y el 23 de febrero de 2020. Todos los pacientes tenían antecedentes de exposición al SARS-CoV-2. Al ingreso, los pacientes no presentaron síntomas y los hallazgos de laboratorio fueron normales. La característica predominante de los hallazgos de la TC fue la opacidad en vidrio esmerilado (GGO, por sus siglas en inglés) (55, 94.8%) con distribución periférica (44, 75.9%) ubicación unilateral (34, 58.6%) y principalmente involucrando uno o dos lóbulos (38, 65,5%) a menudo combinados con línea curvilínea subpleural, reticulación fina, broncograma aéreo, signo de halo o signos de agrandamiento vascular. Después del seguimiento a corto plazo, 16 pacientes (27,6%) presentaron síntomas, con un recuento de linfocitos más bajo y una proteína C reactiva más alta, además de fiebre, tos y fatiga. La evolución de las lesiones en la TC se observó en 10 pacientes (17,2%). El promedio de días de hospitalización fue de 19,80 ± 10,82 días, y fue significativamente mayor en pacientes con progresión de la enfermedad (28,60 ± 7,55 días).
En base a estos resultados, los autores concluyeron que las imágenes de TC de casos asintomáticos con neumonía por COVID-19 tienen características definidas. Debido a que estos pacientes asintomáticos podrían estar generando nuevos brotes e incluso presentar complicaciones en el corto plazo, es esencial la vigilancia de estos pacientes.
Más información:
Heng Meng, Rui Xiong, Ruyuan He, Weichen Lin, Bo Hao, Lin Zhang, Zilong Lu, Xiaokang Shen, Tao Fan, Wenyang Jiang, Wenbin Yang, Tao Li, Jun Chen, Qing Geng. CT imaging and clinical course of asymptomatic cases with COVID-19 pneumonia at admission in Wuhan, China. J Infect, 2020 Jul;81(1): e33-e39. Tomado de:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7152865/pdf/main.pdf
Noticia_Asintomaticos COVID FINAL
Reconstrucción de la dinámica completa de transmisión de COVID-19 en Wuhan
A medida que los países del mundo revisan las intervenciones para contener la pandemia de COVID-19, se pueden extraer lecciones importantes al estudiar la dinámica de transmisión completa del SARS-CoV-2 en Wuhan, China, donde las vigorosas intervenciones no farmacéuticas han suprimido el brote original de COVID-19 local. Aquí, utilizamos un enfoque de modelado para reconstruir el espectro completo de la dinámica de COVID-19 entre el 1 de enero de 2020 y el 8 de marzo de 2020 en cinco períodos marcados por eventos e intervenciones basados en 32,583 casos confirmados por laboratorio. Teniendo en cuenta el índice de contagio presintomática, las tasas de verificación que varían en el tiempo, las tasas de transmisión y los movimientos de población, identificamos dos características clave del brote: alta cobertura y alta transmisibilidad. Estimamos que el 87% (53% de límite inferior) de las infecciones antes del 8 de marzo no fueron detectadas, lo que podría incluir casos asintomáticos y sintomáticos leves; y un número básico de reproducción R0 de 3.54 (95% intervalo creíble [CrI]: 3.40-3.67) en el brote temprano, mucho más alto que para el SARS y MERS. Observamos que las intervenciones múltiples tuvieron efectos positivos considerables en el control del brote, disminuyendo el número de reproducción a 0.28 (0.23-0.33) y por proyección reduciendo las infecciones totales en Wuhan en un 96.0% a partir del 8 de marzo. Además exploramos la probabilidad de resurgimiento después del levantamiento de todas las intervenciones después de 14 días de infecciones no comprobadas, estimándolo en 0,32 y 0,06 basado en modelos con 87% y 53% de infecciones no detectadas, respectivamente, destacando el riesgo que representan los casos no detectados en el cambio de estrategias de intervención. Estos resultados proporcionan implicaciones importantes para la vigilancia continua y las intervenciones para eventualmente contener brotes de COVID-19.
Acceder a documento aquí:
https://www.nature.com/articles/s41586-020-2554-8_reference.pdf
transmisibilidad en wuhan