Análisis computacionales presentan candidatos para tratamiento de Covid19.
La infección con SARS-CoV-2 ha llevado al desarrollo de la pandemia Covid-19 y con ella al estado de emergencia sanitaria mundial. Esto ha generado la urgencia de encontrar tratamientos eficaces mientras se desarrolla una vacuna efectiva para este virus. Diversos medicamentos utilizados en otras patologías están siendo objeto de numerosos estudios clínicos. En general se han encontrado fármacos capaces de inhibir in vitro las proteínas de la envoltura viral, en particular la glicoproteína de la envoltura viral “spike”, y en menor medida otras proteínas dentro de la cápside viral. Sin embargo, aún es muy pronto para conocer los resultados robustos de los estudios clínicos que analizan estos medicamentos.
Científicos de la Universidad de Drexel, en Filadelfia, han decidido estudiar varios tratamientosdisponibles para tratar Covid-19 utilizando la información de secuencia disponible y usando modelos computacionales de homología y acoplamiento molecular in silico. Los análisis se hicieron utilizando los medicamentos que pueden ser efectivos en inhibir el virus a través de su interacción con la glicoproteína spike y con la proteasa 3CL viral.
Ambas proteínas, spike y 3CL, son esenciales para la transmisión y virulencia viral. La inhibición de una de ellas, o de ambas, permitiría reducir ampliamente la severidad de la infección. La proteína spike es capaz de unirse al receptor de membrana celular denominado ACE2 (receptor de la enzima convertidora de angiotensina 2). Dado que no se cuenta con la estructura en forma de cristal de la proteína spike de SARS-CoV-2, para el modelo de homología los científicos utilizaron la estructura cristalina de la proteína spike de SARS-CoV, ya que comparten un 73% de homología. Utilizaron también la secuencia original de SARS-CoV-2, y con la estructura cristalina y la secuencia pudieron modelar la interacción entre esta proteína y los medicamentos estudiados.
Por otra parte, el modelo de acoplamiento molecular in silico se utilizó para estudiar la proteasa 3CL, la cual es responsable de controlar las principales funciones virales como la replicación. Como base de datos utilizaron “Zinc15 database”, que contiene información de diversos antivirales aprobados por agencias de alta vigilancia como FDA.
Los fármacos que se analizaron para estudiar su efectividad en inhibir SARS-CoV-2 fueron NADH, Zanamivir, Bortezomib, Idinavir, Saquinavir, FAD Adeflavin, Coenzima A, Tiludronato, Iomperol, Cangrelor, Carfilzomib y Remdesivir. Los estudios de modelos de homología estudiaron la interacción entre los fármacos y los sitios de unión entre la proteína spike y el receptor ACE2. Pudieron observar que los medicamentos Cangrelor, NADH, Iomeprol, Coenzima A, Tiludronato y FAD Adeflavina (inhibiendo dos sitios de interacción entre ambas moléculas). Estos resultados han sido sorprendentes para los investigadores del proyecto, ya que según el modelo utilizado FAD Adeflavina, que se utiliza para deficiencia de vitamina B2, y Coenzima A, una coenzima, puede ser potencialmente útil para el tratamiento de Covid-19.
Los estudios de acoplamiento molecular in silico demostraron que los antivirales Zanamivir, Idinavir, Saquinavir y Remdesivir son capaces de inhibir la proteasa viral 3CL. Si bien son análisis de modelos computacionales, los resultados parecen ser prometedores ya que estos antivirales están aprobados para su tratamiento de otros virus ARN. Por ejemplo, Zanamivir está aprobado para el tratamiento de Influenza A y B; y por otra parte Indinavir y Sequinavir han sido utilizados para tratar y prevenir el SIDA. Remdesivir ha sido utilizado para tratar SARS, ébola y se está utilizando actualmente para tratar pacientes infectados con SARS-CoV-2.
Sucesivas investigaciones serán requeridas para comprobar lo demostrado por estos modelos computacionales; pero son un buen puntapié para iniciar la búsqueda de evidencia de acción contra SARS-CoV-2 de medicamentos ya utilizados y registrados en las distintas agencias sanitarias del mundo.
Bibliografía:
Hall D et al. A Search for Medications to Treat COVID-19 via in silico Molecular Docking Models of the SARS-CoV-2 Spike Glycoprotein and 3CL Protease. Travel Medicine. 2020. DOI:
https://doi.org/10.1016/j.tmaid.2020.101646
Analisis de tratamientos in vitro para covid por modeling

COPCOV: el estudio clínico que prueba el uso profiláctico de Hidroxicloroquina en COVID-19
Cloroquina e Hidroxicloroquina son medicamentos antipalúdicos utilizados para el tratamiento y profilaxis de la malaria y tratamiento de artritis reumatoidea y lupus eritematoso sistémico. Ambos poseen más de 70 años en el mercado y cuentan con un amplio conocimiento en sus perfiles de seguridad, eficacia y toxicidad.
COPCOV es un estudio fase 3 intervencional, multicéntrico, randomizado (1:1), paralelo, doble ciego, controlado por placebo con 40.000 voluntarios sanos de mayores de 16 años, que trabajan en la salud con contacto con pacientes y que no han sido previamente diagnosticados con COVID-19 y están sanos (NCT04303507). Los brazos de estudio serán dos: (1) placebo y (2) tratamiento con cloroquina (Asia) o hidroxicloroquina (Europa) con una dosis inicial de 10 mg/kg seguido de 155 mg diarios (250 mg de fosfato de cloroquina o 200 mg de sulfato de cloroquina) por 3 meses. Se evaluará el número de casos sintomáticos de COVID-19. Se espera que se inicie en el corriente mes de Abril y finalice en Abril de 2021.
Se espera que este estudio arroje evidencia empírica robusta sobre el uso profiláctico de Cloroquina e Hidroxicloroquina para infecciones de SARS-CoV-2.
Bibliografía:
– Clinical Trials. 2020. Extraído de:
https://clinicaltrials.gov/ct2/show/NCT04320615?term=NCT04320615&draw=2&rank=1

Copcov
COVID-19: resumen de la enfermedad y recomendaciones terapéuticas
Enfermedad
COVID-19 es el tercer brote epidémico de neumonía por coronavirus en lo que va de este siglo, causado por el coronavirus SARS-CoV-2, siendo los brotes anteriores SARS (2003) causado por el virus SARS-CoV y MERS, causado por el virus MERS-CoV (2014).
La acción coordinada de la OMS y la respuesta internacional permitieron contener rápidamente la epidemia de SARS 2003, al igual que la de MERS. En el caso de COVID19 no fue posible contener el brote surgido a fines de diciembre de 2019, declarándose una pandemia el 11 de marzo.
La enfermedad apareció sobre fines de noviembre o comienzos de diciembre de 2019. Al momento de comunicar la aparición del brote, el 31 de diciembre, existían al menos 266 casos diagnosticados.
Al día de hoy el virus SARS-CoV-2 ha infectado a un número no especificado de personas con 2.4 millones de casos confirmados en más de 200 países, 100.000 de los cuales son en Lartinoamérica.
Diagnóstico
La enfermedad COVID-19 se diagnostica mediante RT-PCR (retro-transcriptasa + reacción en cadena de la polimerasa, en tiempo real).
En ausencia de RT-PCR puede sospecharse el diagnóstico cuando existe antecedente epidemiológico y al menos dos de los síntomas leves.
En presencia de síntomas moderados o graves, tales como síndrome respiratorio agudo severo que requiere hospitalización, oxigenoterapia y tratamiento de soporte, con al menos dos de las alteraciones biológicas conocidas tales como el dimero-d aumentado, linfocitopenia, aumento de ferritina, etc.
El diagnóstico serológico es de introducción muy reciente y se utiliza en la evaluación de la inmunidad y en estudios epidemiológicos. En el diagnóstico tiene un 60 a 70% de sensibilidad.
La sensibilidad del test no es de un 100% y debe considerarse falso negativo cuando hay antecedente epidemiológico y síntomas clínicos.
Existen múltiples kits diagnósticos basados en la metodología RT-PCR, los cuales en general no han sido comparados entre sí, habiendo sido aprobados con autorizaciones de emergencia.
Debido a que la cantidad de tests disponibles es limitada o muy limitada, cada país emplea criterios distintos para su administración. El test no se administra de forma universal. Por esta razón, se desconoce el número de personas infectadas por el virus. Sólo se registra el número de personas que han tenido resultado positivo mediante RTPCR para SARS-CoV-2.
En este momento no es posible conocer el número de personas infectadas por el virus; solamente se informan los casos positivos mediante RT-PCR. Al 18 de abril de 2020 se han informado 2.331.000 casos positivos confirmados.
Debido al sesgo introducido por los distintos criterios para la aplicación del test no es posible establecer indicadores epidemiológicos de incidencia, severidad o mortalidad.
Los porcentajes mencionados a continuación se basan en el número de resultados RT-
PCR positivos para SARS-CoV-2
Clínica
El 25% de los pacientes positivos son asintomáticos. En la población general no testeada el porcentaje de infectados asintomáticos no se ha establecido.
El 55% de los pacientes positivos presenta síntomas leves (fiebre, tos seca o con esputo, pérdida del olfato, diarrea, dolor faríngeo, cefalea, náuseas vómitos, dolor articular, congestión nasal, conjuntivitis. También pueden tener neumonitis leve en la radiología o tomografía de tórax.
El 15% de los de los pacientes positivos presenta síntomas moderados. La fiebre se asocia con disnea severa, dificultad respiratoria, taquipnea (> 30 respiraciones / min) e hipoxia (SpO2 <90% en el aire ambiente). En niños puede ocurrir cianosis. En esta definición, el diagnóstico es clínico, y las imágenes radiológicas se usan para excluir complicaciones. Estos pacientes requieren hospitalización durante la fase aguda de la enfermedad.
En el 5% de los casos se presenta enfermedad crítica: insuficiencia respiratoria, shock séptico y/o disfunción orgánica múltiple o falla multiorgánica. Estos pacientes requieren hospitalización, y más de la mitad requiere cuidado intensivo y asistencia respiratoria mecánica.
https://coronavirus.jhu.edu/map.html
Este 5% representa el grupo más desafiante en el tratamiento de la enfermedad. El 50% de estos pacientes mueren debido a distrés respiratorio agudo, sepsis, falla multisistémica, shock y otras causas. Los pacientes que no mueren en general quedan con secuelas importantes.
Patología
En este momento, se considera que el cuadro patológico de los pacientes con COVID19 moderado a severo está dominado por las siguientes alteraciones:
• Respuesta Inmunológica y síndrome de activación macrofágica
• Trombosis
• Daño pulmonar (distrés respiratorio agudo), renal, hepático, cardiovacular y eventualmen-te multiorgánico
• Sepsis
1) Respuesta inmunológica
Durante los meses de febrero/marzo 2020 pudo observarse que los pacientes infectados con Covid-19 moderado a severo presentan datos clínicos y de laboratorio compatibles con el síndrome de Activación Macrofágica o tormenta de citoquinas.
En la fisiopatología del síndrome de activación macrofágica se observa:
• Proliferación incontrolada de las células T.
• Activación excesiva de los macrófagos.
• Hipersecreción de citoquinas proinflamatorias, interleuquina (IL) IL-1β, IL-6, interferón y factor de necrosis tumoral α (TNFα).
Todas estas alteraciones fueron descriptas en pacientes con formas graves de infecciones por SARS-CoV-2.
El aumento de la FERRTINA predice el síndrome de activación macrofágica y la aparición de esta respuesta inmune exagerada.
No existe un tratamiento específico para la respuesta inmunológica. Se está utilizando experimentalmente hidroxicloroquina, tocilizumab, dexametasona, interferón, remdesivir, ritonavir/lopinavir, metotrexato, etc.
La enoxaparina puede contribuir en este aspecto por sus propiedades anti-IL6.
2) Trombosis
Acompañando a la respuesta macrofágica descontrolada, se encuentra en estos pacientes una activación patológica de la trombina, observándose episodios trombóticos que van desde isquemia periférica y tromboembolismo pulmonar hasta coagulación intravascular diseminada (CID). Estas complicaciones fueron la causa de muerte en muchos de estos enfermos. El parámetro de laboratorio más apropiado para reconocer este estado trombofílico es el DIMERO D elevado, por lo cual se sugiere su medición en todos los pacientes hospitalizados.
El concepto de inmuno-trombosis describe la interacción entre el sistema inmune y el sistema de coagulación como respuesta a la infección. Cuando se activan estos mecanismos, como consecuencia de una infección sistémica, se produce el cuadro de coagulación intravascular diseminada (CID), caracterizada por la presencia de depósitos masivos de fibrina en la circulación, lo que conlleva daño orgánico y empeora el pronóstico de los pacientes. Diversos estudios han demostrado un nexo entre la severidad de la coagulopatía, la disfunción orgánica y la mortalidad en pacientes con sepsis.
La trombosis y la coagulación intravascular diseminada pueden prevenirse mediante el empleo de heparinas de bajo peso molecular como enoxaparina y antagonistas directos como Apixaban.
Las heparinas, incluyendo la enoxaparina, tiene propiedades antiinflamatorias incluyendo la inhibición de IL6 y del sistema de activación macrofágica. De este modo, las heparinas ayudan a corregir la respuesta trombótica y la respuesta inmune causada por la infección por SARS-CoV-2.
Las heparinas, especialmente las de bajo peso molecular como enoxaparina, figuran hoy día en la primera línea de tratamiento de COVID-19, en todos los protocolos y guias terapéuticas incluyendo la guía que utiliza la OMS, que reproduce la del Grupo de Trabajo sobre Hemostasia de la Sociedad Suiza de Hematología que reproducimos más abajo. La OMS recomienda el empleo de heparina subcutánea desde fines de enero.
La enoxaparina puede tener indicación en un 5 a 10% de los pacientes COVID-19, durante un período limitado.
La tromboprofilaxis reduce la formación de trombos y puede evitar la coagulación intravascular diseminada. Aunque la tromboprofilaxis reduce la mortalidad, no evita las secuelas y no resuelve la totalidad del cuadro clínico.
El empleo de heparina en los pacientes con COVIS19 severo es una recomendación clara del Consenso de Expertos de Shanghai http://rs.yiigle.com/m/yufabiao/1183266 .htm
3) Daño pulmonar
Las autopsias a pacientes fallecidos por COVID19 realizadas en China, Italia y Estados Unidos muestra resultados similares.
https://jcp.bmj.com/content/early/2020/04/01/jclinpath-2020-206522
https://www.nature.com/articles/s41379-020-0536-x
https://www.medrxiv.org/content/10.1101/2020.04.06.20050575v1
Según los resultados, macroscópicamente los pulmones aparecen aumentados de peso, con consistencia aumentada, manchados con áreas hiperémicas/hemorrágicas alternando con áreas rosadas.
Histológicamente, algunas áreas son severamente enfisematosas, con vasos sanguíneos muy dilatados, presencia de trombos y microtrombos. En muchos casos, el daño alveolar difuso es evidente, con descamación de neumocitos, formación de membranas hialinas, células multinucleadas y un exudado fibrótico intra-alveolar.
El daño pulmonar produce disnea, que puede evolucionar a hipoxemia refractaria a la asistencia respiratoria mecánica con PEEP y shock.
No existe un tratamiento específico para el daño pulmonar. La enoxaparina puede prevenir el daño pulmonar de causa trombótica. La asistencia respiratoria mecánica es un tratamiento de sostén. El período durante el cual el paciente puede requerir asistencia respiratoria mecánica es muy variable y puede superar los 20 días.
La asistencia respiratoria requiere el empleo de fármacos sedativos tales como MIDAZOLAM y FENTANILO que se emplean por vía intravenosa o mediante bomba de infusión, y fármacos curarizantes como PANCURONIO o ROCURONIO.
Los chinos han empleado interferón beta inhalatorio en pacientes con ventilación asistida, al parecer sin resultado en las fases avanzadas de la enfermedad.
4) Sepsis
La respuesta inmune desregulada también tiene una etapa de supresión inmune que sigue a la fase proinflamatoria. Se caracteriza por reducción sustancial de los linfocitos periféricos, principalmente células T CD4 y CD8 y se asocia con un alto riesgo de desarrollar infección bacteriana secundaria.
https://www.thelancet.com/action/showPdf?pii=S0140-6736%2820%2930920-X
Esta condición, conocida como linfopenia, también se encontró en influenza severa y otras infecciones virales respiratorias. Se ha demostrado que la linfopenia se correlaciona con la gravedad de COVID-19. El mecanismo subyacente se desconoce. Estudios previos han demostrado que las partículas virales similares al SARS y el ARN del SARS-CoV fueron detectados en linfocitos T aislados de muestra de sangre, bazo, ganglios linfáticos y tejido linfoide de varios órganos, sugiriendo que el SARS-CoV podría ser capaz de infectar células T directamente.
El ARN del SARS-CoV-2 también se detectó en muestras de sangre. Por lo tanto, es razonable suponer que, además de la muerte celular inducida por la activación, así como la relacionada con TNF, SARS-CoV-2 podría infectar directamente los linfocitos, particularmente las células T, e iniciar o promover la muerte celular de los linfocitos, que eventualmente conduce a linfopenia y alteración de la respuesta antiviral. Se desconce si los macrófagos alveolares pueden fagocitar la partícula viral.
El tratamiento de la sepsis consiste en antivirales tales como remdesivir, lopinavir/ritonavir, favipiravir, etc. y antibióticos tales como ceftrixona
Para la hidroxicloroquina se plantea una acción moduladora de la inflamación y también antiviral. Ambas acciones han sido demostradas in vitro. Todavía no se dispone de datos confiables provenientes de los estudios clínicos que se están llevando a cabo con HQ.
Prevención primaria del contagio de COVID-19
Además del distanciamiento, el uso de máscaras y el alcohol, se han planteado varias alternativas farmacológicas para prevenir la transmisión.
Existen varios estudios en curso a nivel global para evaluar la prevención primaria del contagio en personal sanitario.
Entre los fármacos que se están estudiando figuran:
-hidroxicloroquina
-remdesivir
-vacuna BCG
-vitamina D
-flavonoides (tales como isoquercitina e isoflavonas)
Estos estudios han comenzado en el mes de abril y no se esperan resultados antes junio.
Recomendaciones de la OMS-OPS
Sugerencias para tromboprofilaxis y monitoreo paraclínico en pacientes con COVID19 hospitalizados
La creciente evidencia de múltiples cohortes retrospectivas indica que los pacientes hospitalizados con COVID-19 pueden sufrir una activación de coagulación excesiva que conduce a un mayor riesgo de trombosis venosa y arterial (incluidos los vasos de pequeño calibre) y un curso clínico deficiente.
En particular, el nivel de dímero D en el momento del ingreso al hospital es un predictor del riesgo de desarrollar síndrome de distrés respiratorio agudo (SDRA), del riesgo de ingreso en cuidados intensivos y del riesgo de muerte.
Un estudio observacional en pacientes con COVID-19 con niveles elevados de dímero D al inicio del estudio mostró que la mortalidad a los 28 días fue menor en los que recibieron heparina que en los que no recibieron. Basado en la literatura disponible y las recomendaciones publicadas de la Sociedad Internacional de Trombosis y Hemostasia https://www.isth.org, de la Sociedad Americana de Hematología https://www.hematology.org/covid-19 y de la Sociedad para la Investigación de Trombosis y Hemostasia http://gth-online.org, el Grupo de Trabajo sobre Hemostasia de la Sociedad Suiza de Hematología propone las siguientes recomendaciones para la tromboprofilaxis farmacológica en pacientes con COVID-19 en el contexto agudo. Las sugerencias se actualizarán periódicamente.
- Todos los pacientes hospitalizados con COVID-19 deben recibir tromboprofilaxis farmacológica de acuerdo con una estratificación de riesgo, a menos que esté contraindicado.
- En pacientes con aclaramiento de creatinina> 30 ml / min, la heparina de bajo peso molecular (HBPM) debe administrarse de acuerdo con la información de prescripción. Se debe considerar un aumento de la dosis en pacientes con sobrepeso (> 100 kg).
- En pacientes con aclaramiento de creatinina <30 ml / min, debe administrarse heparina no fraccionada por vía subcutánea dos veces o tres veces al día o por vía intravenosa o se debe administrar de acuerdo con la información de prescripción. Se debe considerar un aumento de la dosis en pacientes con sobrepeso (> 100 kg).
- La actividad anti-Xa debe monitorearse cuando se indique (p. ej., evidencia de disfunción renal).
- La antitrombina no necesita ser monitoreada pero esto podría ser considerado de forma individual en casos de coagulación intravascular diseminada o coagulopatía inducida por sepsis o resistencia a la heparina.
- Sugerimos monitorear regularmente el tiempo de protrombina, dinero-D, fibrinógeno, recuento de plaquetas, lactato deshidrogenasa (LDH), creatinina y alanina aminotransferasa (ALT) (diariamente o al menos 2−3 veces por semana).
- En pacientes en cuidados intensivos con un gran aumento de dinero D, inflamación severa o signos de disfunción hepática o renal o insuficiencia respiratoria inminente, deben considerarse dosis intermedia o terapéutica de HBPM o UHF, de acuerdo con el riesgo de sangrado.
- La trombocitopenia inducida por heparina (HIT) debe ser considerada en pacientes con fluctuaciones en recuento de plaquetas o signos de resistencia a la heparina.
Conexion Megalabs - COVID-19 resumen de la enfermedad y recomendaciones terapéuticas

Se descubre nuevo anticuerpo contra el virus SARS-CoV-2
En el período comprendido entre los años 2002-2003 tuvo lugar la epidemia con el virus SARS-CoV, que afectó más de 17 países. Un sobreviviente de dicha epidemia fue quién aportó la muestra biológica para que Ter Meulen y colaboradores encontraran el anticuerpo CR3022 en 2006. Este anticuerpo es capaz de unirse a la proteína de la envoltura de SARS-CoV llamada “spike”, por su aspecto de espina al ser observada a través de microscopía electrónica. Esta proteína es clave para que el virus pueda ingresar a la célula.
La proteína spike de SARS-CoV y de SARS-CoV-2 comparten el 77% de la estructura primaria. Dicha similitud fue la que impulsó a Tian X y colaboradores a analizar si el anticuerpo CR3022 también es capaz de unirse con buena afinidad a la proteína spike de SARS-CoV-2. Además de confirmarlo, los autores establecieron la importancia del hallazgo, dado que algunos de los potentes anticuerpos que se han hallado para SARS-CoV han fallado en unirse a la proteína spike de SARS-CoV-2.
Yuan y colaboradores recientemente analizaron la unión entre el virus y el anticuerpo con resolución atómica nuclear. Observaron que CR3022 no compite con el sitio de unión a la célula del receptor celular ACE2 (enzima convertidora de angiotensina I-2; como ocurre con otros anticuerpos), sino que actúa por otro mecanismo. La proteína spike es capaz de estar en dos conformaciones, análogamente como un “switch” de una llave eléctrica, puede estar “on” y “off”. Spike solamente es capaz de unirse al receptor ACE2 si está en su conformación “on” y ocurre de igual forma con el anticuerpo CR3022. Cuando CR3022 se une a la proteína Spike, hace que ésta última cambie de conformación y pase a su estado “off”, impidiendo así que se una con el receptor ACE2.
Mediante estudios in vitro se observó que si bien CR3022 no neutraliza completamente a SARS-CoV-2, es capaz de colaborar en su tratamiento. Su utilización en una posible vacuna para SARS-CoV-2 requiere aún más análisis, pero estos hallazgos resultan alentadores para la comunidad científica.
Bibliografía:
– Yuan M et al. A highly conserved cryptic epitope in the receptor-binding domains of SARS-CoV-2 and SARS-CoV. Science . 2020. eabb7269. Doi: 10.1126/science.abb7269.
– Tian X et al. Potent binding of 2019 novel coronavirus spike protein by a SARS coronavirus-specific human monoclonal antibody. Emergin Microbes & Infections. 2020. 9 (1). Doi: 10.1080/22221751.2020.1729069
Conexion Megalabs - Se descubre nuevo anticuerpo contra el virus SARS-CoV-2

Pérdida de funcionalidad sensorial en pacientes asintomáticos con COVID-19.
Los síntomas usuales de personas infectadas con SARS-CoV-2 suelen ser fiebre, tos y dificultad para respirar. Sin embargo, hay un 18% de las personas infectadas que son asintomáticas o poseen síntomas mínimos. Recientemente estudios preliminares en Irán e Italia observaron que en casos asintomáticos o leves de infección con Covid-19, los pacientes reportaron pérdida de gusto y olfato.
Desórdenes en el gusto y olfato han sido reportados en diversas infecciones virales, y en particular se ha demostrado en un modelo en ratones infectados con SARS-CoV penetración transneural a través del bulbo olfatorio. Las células epiteliales de las mucosas orales y nasales poseen una alta concentración del receptor celular ACE2 (enzima convertidora de angiotensina I-2), receptor utilizado por los virus SARS-CoV y SARS-CoV-2. Esta evidencia podría comenzar a explicar el mecanismo patogénico que subyace a las afecciones en el gusto y el olfato en pacientes con COVID-19. Sin embargo, los mecanismos moleculares por los cuales esto ocurre aún no es esclarecido.
Un estudio clínico transversal fue realizado con 1480 pacientes con síntomas de tipo gripal para evaluar los sentidos de olfato y gusto en pacientes asintomáticos con Covid-19 o casos leves. Mediante PCR se vio que 102 casos fueron positivos para SARS-CoV-2. Todos los pacientes recibieron un cuestionario con 27 preguntas relacionadas al olfato y gusto en distintos días, con una escala del 0-10 (0: sin percepción del olfato/gusto; 10: normal percepción del olfato/gusto). Las respuestas que fueron analizadas estadísticamente mediante el test de Chi cuadrado, con un intervalo de confianza del 95%. Los resultados mostraron que en el 68% de los casos se observó alteración en el sentido del olfato, y en el 71% de los casos se observó alteración en el sentido del gusto. El 74% de los pacientes infectados con Covid-19 mostraron mejoras de ambos síntomas (18% antes de la semana 1, un 38% entre la semana 1 y 2, y un 18% entre la semana 2 a 4).
Este estudio demostró que, en pacientes con sintomatología similar, aquellos casos positivos para Covid-19 mostraron pérdida de olfato y gusto durante el transcurso de la infección. Estudios a mayor escala serán necesarios para poder determinar la incidencia y prevalencia de anosmia e hiposmia entre los casos positivos de SARS-CoV-2.
Bibliografía:
– Yan CH1, Faraji F1, Prajapati DP1,2, Boone CE3, DeConde AS1. Association of chemosensory dysfunction and Covid-19 in patients presenting with influenza-like symptoms. Int Forum Allergy Rhinol. 2020. Doi: 10.1002/alr.22579.
– Giacomelli A et al. Self-reported olfactory and taste disorders in SARS-CoV-2 patients: a cross-sectional study. Clin. Infec. Dis. 2020. Ciaa330. Doi: 10.1093/cid/ciaa330

Conexion Megalabs - Perdida de funcionalidad sensorial en pacientes asintomaticos con COVID-19
Hidroxicloroquina
La Hidroxicloroquina es un fármaco que pertenece al grupo de medicamentos denominados antipalúdicos y también a los antirreumáticos modificadores de la enfermedad (FAME). Este fármaco fue aprobado en el año 1955 por la FDA y en el año 1958 en Europa (Finlandia)(13), (14). Está indicado en el tratamiento de artritis reumatoide aguda o crónica, tratamiento de lupus eritematoso sistémico (LES) y discoide crónico, y para la prevención y tratamiento de malaria (paludismo) no complicada causada por especies de plasmo-dio sensibles (Plasmodium vivax, P. malariae, P. ovale y cepas susceptibles de P. falciparum), cuando no resulten adecuados o no estén disponibles otros tratamientos. (2)
Dosis y administración propuestas para COVID-19 (1)
Hidroxicloroquina
Adultos
Hidroxicloroquina sulfato: 400 mg cada 12 horas el día 1 seguido de 200 mg cada 12 horas oral. La duración será individualizada; inicialmente tratar durante al menos 5 días con una duración máxima de 14 días.
Precauciones y advertencias
• General: se debe usar con precaución en pacientes con trastornos gastrointestinales, neurológicos o sanguíneos, y en aquellos con sensibilidad a la quinina.
• Enfermedad hepática/renal: deben usarse con precaución en pacientes con enfermedad hepática o alcoholismo o en combinación con fármacos hepatotóxicos conocidos.
• Efectos hematológicos/pruebas de laboratorio: se deben realizar recuentos periódicos de células sanguíneas si los pacientes reciben terapia prolongada.
• Debe administrarse con precaución en pacientes con deficiencia de glucosa-6-fosfato deshidrogenasa (G-6-PD).
• Efectos dermatológicos: se debe tener especial precaución cuando se administra a cualquier paciente que reciba un medicamento con una tendencia significativa a producir dermatitis.
• Cepas resistentes de la malaria: no es eficaz contra las cepas de P. falciparum resistentes a la cloroquina.
• Sistema visual: se ha observado daño irreversible de la retina en algunos pacientes que recibieron sulfato de Hidroxicloroquina. Se debe realizar un examen oftalmológico inicial dentro del primer año de inicio de este medicamento
• Efectos cardíacos, incluida la cardiomiopatía y la prolongación del intervalo QT: se han notificado casos de cardiomiopatía mortal y potencialmente mortal con el uso posterior a la comercialización de Hidroxicloroquina y con el uso de Cloroquina. Los pacientes pueden presentar bloqueo auriculoventricular, hipertensión pulmonar, síndrome del seno enfermo o complicaciones cardíacas. Se recomienda la monitorización clínica de signos y síntomas de cardiomiopatía, incluido el uso de herramientas de diagnóstico apropiadas, para controlar a los pacientes en busca de cardiomiopatía durante el tratamiento con este medicamento. No debe administrarse con otros medicamentos que tengan el potencial de prolongar el intervalo QT.
• Agravamiento de la psoriasis y la porfiria: el uso de Hidroxicloroquina en pacientes con psoriasis puede precipitar un ataque severo de psoriasis. Cuando se usa en pacientes con porfiria, la afección puede exacerbarse.
• Miopatía y neuropatía proximal: se ha reportado debilidad progresiva y atrofia de los grupos musculares proximales, reflejos tendinosos deprimidos y conducción nerviosa anormal producida por miopatía o neuropatía del músculo esquelético.
• Eventos neuropsiquiátricos, incluyendo suicidio: rara vez se ha informado de comportamientos suicidas en pacientes tratados con Hidroxicloroquina.
• Hipoglucemia: se ha demostrado que Hidroxicloroquina causa hipoglucemia severa, incluida la pérdida de conciencia, que podría ser mortal en pacientes tratados con o sin medicamentos antidiabéticos.
Eventos adversos (2)
Trastornos oculares reversibles tras interrumpir el tratamiento de forma temprana. Pérdida del apetito y de peso. Náuseas, diarrea. Otras reacciones con frecuencia desconocida o rara podrían ser: hipoglucemia tanto en pacientes que están tomando o no medicamentos antidiabéticos, cefalea, sordera, acúfenos, alteración de la función hepática.
Estudios clínicos con COVID-19
• Efficacy and Safety of Hydroxychloroquine for Treatment of Pneumonia Caused by 2019-nCoV ( HC-nCoV). (3)

• Comparison of Lopinavir/Ritonavir or Hydroxychloroquine in Patients With Mild Coronavirus Disease (COVID-19). (4)
• Safety and Efficacy of Hydroxychloroquine Associated With Azithromycin in SARS-CoV2 Virus (Coalition Covid-19 Brasil II). (5)
• Chloroquine/ Hydroxychloroquine Prevention of Coronavirus Disease (COVID-19) in the Healthcare Set-ting (COPCOV). (6)
• Hydroxychloroquine Chemoprophylaxis in Healthcare Personnel in Contact With COVID-19 Patients (PHYDRA Trial) (PHYDRA). (7)
• Hydroxychloroquine Post Exposure Prophylaxis for Coronavirus Disease (COVID-19). (8)
• Hydroxychloroquine Treatment for Severe COVID-19 Pulmonary Infection (HYDRA Trial) (HYDRA). (9)
• Various Combination of Protease Inhibitors, Oseltamivir, Favipiravir, and Hydroxychloroquine for Treat-ment of COVID19 : A Randomized Control Trial (THDMS-COVID19). (10)

Inserto del producto
(Archivo descargable)
(1) Tratamientos disponibles para el manejo de la infección respiratoria por SARS-CoV-2. AEMPS2020.
Available from: https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/tratamientos-disponibles-para-el-manejo-de-la-infeccion-respiratoria-por-sars-cov-2/.
(2) Inserto Plaquenil: Food and Drug Administration; 2019.
Available from: https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/009768Orig1s051lbl.pdf
(3) Efficacy and Safety of Hydroxychloroquine for Treatment of Pneumonia Caused by 2019-nCoV ( HC-nCoV ) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04261517.
(4) Comparison of Lopinavir/Ritonavir or Hydroxychloroquine in Patients With Mild Coronavirus Dis-ease (COVID-19) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04307693.
(5) Safety and Efficacy of Hydroxychloroquine Associated With Azithromycin in SARS-CoV2 Virus (Coalition Covid-19 Brasil II) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04321278.
(6) Chloroquine/ Hydroxychloroquine Prevention of Coronavirus Disease (COVID-19) in the Healthcare Setting (COPCOV). ClinicalTrials.gov: NIH. US National Library of Medicine.; 2020.
Avail-able from: https://clinicaltrials.gov/ct2/show/NCT04303507.
(7) Hydroxychloroquine Chemoprophylaxis in Healthcare Personnel in Contact With COVID-19 Pa-tients (PHYDRA Trial) (PHYDRA) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04318015.
(8) Hydroxychloroquine Post Exposure Prophylaxis for Coronavirus Disease (COVID-19) 2020.
Availa-ble from: https://clinicaltrials.gov/ct2/show/NCT04318444.
(9) Hydroxychloroquine Treatment for Severe COVID-19 Pulmonary Infection (HYDRA Trial) (HYDRA) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04315896.
(10) Various Combination of Protease Inhibitors, Oseltamivir, Favipiravir, and Hydroxychloroquine for Treatment of COVID19 : A Randomized Control Trial (THDMS-COVID19) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04303299.
Conexión-Hidroxicloroquina
Lopinavir/Ritonavir
El Lopinavir/Ritonavir es un inhibidor de la proteasa del VIH-1 indicado en combinación con otros agentes antirretrovirales para el tratamiento de la infección por VIH-1 en adultos y pacientes pediátricos. Ha sido aprobado por la FDA en 2006. (6)
Dosis y administración propuestas para COVID-19 (1)
Adultos
• Lopinavir/Ritonavir 200 mg/100 mg comprimidos: la dosis es 400/100mg (2 comprimidos) cada 12 horas vía oral. La duración será individualizada, pudiendo utilizarse de guía para la retirada la desa-parición de la fiebre, y la duración máxima será de 14 días.
• Lopinavir/Ritonavir 80/20 mg/ml solución oral: la dosis es 400/100mg (5 ml) cada 12 horas vía ad-ministración por sonda. La solución debe reservarse para pacientes intubados en cuidados inten-sivos y para la población pediátrica que no sea subsidiaria de tratamiento con los comprimidos, ya sea porque la dosis es inapropiada o por las dificultades para tragar los mismos.
Pediátrico
• Pacientes pediátricos desde los 14 días hasta los 6 meses: 16/4 mg/kg/dosis (corresponde a 0,2 mL/kg), 2 veces al día o 300/75 mg/m2 dosis (corresponde a 3,75 mL/m2), 2 veces al día.
• Pacientes pediátricos desde los 6 meses hasta los 18 años:
o 7 a 15 kg 12/3 mg/kg/dosis, 2 veces/día.
o 15-40 kg 10/2.5 mg/kg/dosis, 2 veces/día.
o >40 kg: 400 /100 mg (200 mg/50 mg por cápsula), dos cápsulas (o 5 mL de la solu-ción), 2 veces/día.
Precauciones y advertencias (2)
• Toxicidad en neonatos prematuros: no debe usarse en neonatos prematuros en el período pos-natal inmediato debido a posibles toxicidades. No se ha establecido una dosis segura y efectiva de solución oral en esta población de pacientes.
• Pancreatitis
• Hepatotoxicidad: monitorer la función hepática antes y durante la terapia, especialmente en pa-cientes con enfermedad hepática subyacente, incluyendo hepatitis B y hepatitis C, o elevaciones marcadas de transaminasas.
• Se han informado casos de prolongación del intervalo QT y casos aislados de torsade de pointes.
• La prolongación del intervalo PR puede ocurrir en algunos pacientes. Usar con precaución en pa-cientes con enfermedad del sistema de conducción preexistente, cardiopatía isquémica, miocar-diopatía, cardiopatía estructural subyacente o cuando se administra con otros medicamentos que pueden prolongar el intervalo PR.
• Los pacientes pueden desarrollar un nuevo inicio o exacerbaciones de diabetes mellitus, hiperglu-cemia, síndrome de reconstitución inmune, redistribución/acumulación de grasa corporal.
• Elevaciones totales de colesterol y triglicéridos. Monitorear antes de la terapia y periódicamente después.
• Hemofilia: puede producirse un sangrado espontáneo y puede ser necesario factor VIII adicional.
Eventos adversos (2)
Frecuentes: diarrea, náuseas, vómitos, hipertrigliceridemia e hipercolesterolemia. Infrecuentes: pancreatitis, prolongación del segmento QT del electrocardiograma.
Su uso puede implicar serios eventos adversos a nivel de páncreas e hígado, observándose casos de pancreatitis y hepatotoxicidad, llegando a incluir resultados fatales.
Estudios clínicos con COVID-19
• Trial of Treatments for COVID-19 in Hospitalized Adults (DisCoVeRy). (3)
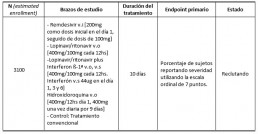
• Comparison of Lopinavir/Ritonavir or Hydroxychloroquine in Patients With Mild Coronavirus Dis-ease (COVID-19). (4)

• Lopinavir/ Ritonavir, Ribavirin and IFN-beta Combination for nCoV Treatment. (5)

• COVID-19 Ring-based Prevention Trial With Lopinavir/Ritonavir (CORIPREV-LR). (6)
• Evaluating and Comparing the Safety and Efficiency of ASC09/Ritonavir and Lopinavir/Ritonavir for Novel Coronavirus Infection. (7)

• Multicenter Clinical Study on the Efficacy and Safety of Xiyanping Injection in the Treatment of New Coronavirus Infection Pneumonia (General and Severe). (8)
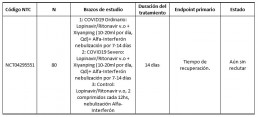
• The Clinical Study of Carrimycin on Treatment Patients With COVID-19. (9)

Link a información del producto de FDA:
www.accessdata.fda.gov/drugsatfda_docs/label/2019/021251s058,021906s053lbl.pdf.
(1) Tratamientos disponibles para el manejo de la infección respiratoria por SARS-CoV-2. AEMPS2020.
Available from: https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/tratamientos-disponibles-para-el-manejo-de-la-infeccion-respiratoria-por-sars-cov-2/.
(2) Inserto Kaletra Food and Drug Administration2019.
Available from: https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/021251s058,021906s053lbl.pdf.
(3) Trial of Treatments for COVID-19 in Hospitalized Adults (DisCoVeRy). 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04315948.
(4) Comparison of Lopinavir/Ritonavir or Hydroxychloroquine in Patients With Mild Coronavirus Dis-ease (COVID-19) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04307693.
(5) Lopinavir/ Ritonavir, Ribavirin and IFN-beta Combination for nCoV Treatment 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04276688.
(6) COVID-19 Ring-based Prevention Trial With Lopinavir/Ritonavir (CORIPREV-LR) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04321174.
(7) Evaluating and Comparing the Safety and Efficiency of ASC09/Ritonavir and Lopinavir/Ritonavir for Novel Coronavirus Infection 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04261907.
(8) Multicenter Clinical Study on the Efficacy and Safety of Xiyanping Injection in the Treatment of New Coronavirus Infection Pneumonia (General and Severe 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04295551.
(9) The Clinical Study of Carrimycin on Treatment Patients With COVID-19 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04286503.
Conexión_Lopinavir Ritonavir
Interferón beta-1A
El Interferón-beta-1 A está indicado para el tratamiento de formas recurrentes de esclerosis múltiple (EM), que incluye síndrome clínicamente aislado, enfermedad recurrente y enfermedad secundaria activa progresiva, en adultos. Fue aprobado por la Agencia estadounidense en el año 2002. (2)
Dosis y administración propuestas para COVID-19 (1)
Adultos
5 millones de unidades agregando 2 mL de suero estéril, dos veces al día inhalado. Nebulización con interferón-α2b 100.000–200.000 UI/kg para casos leves, y 200.000–400.000 UI/kg para casos graves, dos veces al día durante 5–7 días.
Pediátrica
Nebulización de 100.000-200.000 UI/kg para casos leves; 200.000-400.000 UI/kg en casos graves, dos veces / día durante 5-7 días
Precauciones y advertencias (2)
• Depresión y suicidio: se aconseja discontinuar el tratamiento ante sintomas de depresión.
• Lesión hepática: se recomienda controlar las pruebas de función hepática; vigilar a los pacientes en busca de signos y síntomas de lesión hepática; considere suspender REBIF si la lesión hepática ocurre
• Anafilaxia y otras reacciones alérgicas:
• Reacciones en el lugar de inyección, incluida la necrosis:
• Disminución de los recuentos sanguíneos periféricos: controle los recuentos sanguíneos completos
• Microangiopatía trombótica
• Convulsiones: se recomienda controlar las convulsiones, particularmente aquellos con trastornos convulsivos preexistentes
Eventos adversos
Anorexia, depresión, insomnio, ansiedad, labilidad emocional, mareo, cefalea, náuseas, vómitos, diarrea, dolor abdominal, alopecia, rash, mialgia, artralgia, dolor musculoesquelético, inflamación y reacción en punto de inyección, fatiga, rigidez, pirexia, síntomas pseudogripales, malestar general, irritabilidad
Entre las reacciones adversas notificadas con mayor frecuencia para este medicamento se encuentran los síntomas similares a la gripe (ocurrió en 59% de los participantes del estudio clínico realizado para Rebif con una dosis de 44mcg) y elevaciones en las enzimas hepáticas.
Estudios clínicos con COVID-19
• Trial of Treatments for COVID-19 in Hospitalized Adults (DisCoVeRy). (17)

• Experimental Trial of rhIFNα Nasal Drops to Prevent 2019-nCOV in Medical Staff. (29)

• Evaluating the Efficacy and Safety of Bromhexine Hydrochloride Tablets Combined With Standard Treat-ment/ Standard Treatment in Patients With Suspected and Mild Novel Coronavirus Pneumonia (COVID-19). (30)

• Lopinavir/ Ritonavir, Ribavirin and IFN-beta Combination for nCoV Treatment. (20)

Link a información del producto de FDA:
www.accessdata.fda.gov/drugsatfda_docs/label/2019/103780s5204lbl.pdf
(1) Tratamientos disponibles para el manejo de la infección respiratoria por SARS-CoV-2. AEMPS2020.
Available from: https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/tratamientos-disponibles-para-el-manejo-de-la-infeccion-respiratoria-por-sars-cov-2/.
(2) Inserto Rebif Food and Drug Administration2019.
Available from: https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/103780s5204lbl.pdf.
(3) Trial of Treatments for COVID-19 in Hospitalized Adults (DisCoVeRy). 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04315948.
(4) Experimental Trial of rhIFNα Nasal Drops to Prevent 2019-nCOV in Medical Staff 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04320238.
(5) Evaluating the Efficacy and Safety of Bromhexine Hydrochloride Tablets Combined With Standard Treatment/ Standard Treatment in Patients With Suspected and Mild Novel Coronavirus Pneu-monia (COVID-19) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04273763.
(6) Lopinavir/ Ritonavir, Ribavirin and IFN-beta Combination for nCoV Treatment 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04276688.
Conexion_Interferon beta
Interferón alfa-2B
El Interferón-alfa-2B es un antiviral indicado para el tratamiento de la hepatitis crónica C (CHC) en pacientes con enfermedad hepática compensada.
Fue aprobado por la FDA en el año 2001. (2)
Dosis y administración propuestas para COVID-19(1)
Adultos
Dosis: 250 microgramos administrados por vía subcutánea cada 48 h durante 14 días.
Precauciones y advertencias (2)
Si se administra con ribavirina, las advertencias y precauciones para la ribavirina también se aplican a este régimen combinado. Los pacientes que exhiben las siguientes condiciones deben ser monitoreados de cerca y pueden requerir una reducción de la dosis o la interrupción de la terapia:
• Eventos neuropsiquiátricos.
• Historia de enfermedad cardíaca significativa o inestable.
• Hipotiroidismo, hipertiroidismo, hiperglucemia, diabetes mellitus que no pueden tratarse eficaz-mente con medicamentos.
• Trastornos oftalmológicos nuevos o que empeoran.
• Eventos cerebrovasculares isquémicos y hemorrágicos.
• Disminuciones severas en el recuento de neutrófilos o plaquetas.
• Historia de trastornos autoinmunes.
• Pancreatitis y colitis y pancreatitis ulcerosa o hemorrágica / isquémica.
• Infiltrados pulmonares o deterioro de la función pulmonar.
• Puntaje de Child-Pugh mayor a 6 (clase B y C).
• Aumento de los niveles de creatinina en pacientes con insuficiencia renal.
• Reacciones graves de hipersensibilidad aguda y erupciones cutáneas.
• Trastornos dentales / periodontales informados con terapia combinada.
• Pérdida de peso e inhibición del crecimiento informada durante la terapia combinada en pacien-tes pediátricos.
• Inhibición del crecimiento a largo plazo (altura)
• Neuropatía periférica cuando se usa en combinación con telbivudina.
Eventos adversos (2)
Fiebre, cefalea, hipertonía, miastenia, rash, náusea, diarrea, linfopenia, leucopenia, reacción local, debilidad, artralgia, síndrome pseudogripal.
Los riesgos a destacar asociado a este medicamento son los desórdenes pulmonares, los cuales incluyen infiltrados pulmonares, neumonía, disnea, bronquiolitis obliterante, neumonitis intersticial, hipertensión pulmonar, sarcoidosis e insuficiencia respiratoria.
Estudios clínicos con COVID-19
• Evaluation of Ganovo (Danoprevir ) Combined With Ritonavir in the Treatment of Novel Coronavirus Infection. (3)
• Experimental Trial of rhIFNα Nasal Drops to Prevent 2019-nCOV in Medical Staff. (4)

• Evaluating the Efficacy and Safety of Bromhexine Hydrochloride Tablets Combined With Standard Treat-ment/ Standard Treatment in Patients With Suspected and Mild Novel Coronavirus Pneumonia (COVID-19). (5)
• A Prospective/Retrospective,Randomized Controlled Clinical Study of Interferon Atomization in the 2019-nCoV Pneumonia. (6)

• Efficacy and Safety of INF-α2β in the Treatment of Novel Coronavirus Patients (7)

• Multicenter Clinical Study on the Efficacy and Safety of Xiyanping Injection in the Treatment of New Coronavirus Infection Pneumonia (General and Severe). (8)

Link a información del producto de FDA:
www.accessdata.fda.gov/drugsatfda_docs/label/2019/103949s5313lbl.pdf.
(1) Tratamientos disponibles para el manejo de la infección respiratoria por SARS-CoV-2. AEMPS2020.
Available from: https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/tratamientos-disponibles-para-el-manejo-de-la-infeccion-respiratoria-por-sars-cov-2/.
(2) Inserto Pegintron Food and Drug Administration2019.
Available from: https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/103949s5313lbl.pdf.
(3) Evaluation of Ganovo (Danoprevir) Combined With Ritonavir in the Treatment of Novel Corona-virus Infection 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04291729.
(4) Experimental Trial of rhIFNα Nasal Drops to Prevent 2019-nCOV in Medical Staff 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04320238.
(5) Evaluating the Efficacy and Safety of Bromhexine Hydrochloride Tablets Combined With Standard Treatment/ Standard Treatment in Patients With Suspected and Mild Novel Coronavirus Pneu-monia (COVID-19) 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04273763.
(6) A Prospective/Retrospective,Randomized Controlled Clinical Study of Interferon Atomization in the 2019-nCoV Pneumonia. 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04254874.
(7) Efficacy and Safety of INF-α2β in the Treatment of Novel Coronavirus Patients.(2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04293887.
(8) Multicenter Clinical Study on the Efficacy and Safety of Xiyanping Injection in the Treatment of New Coronavirus Infection Pneumonia (General and Severe 2020.
Available from: https://clinicaltrials.gov/ct2/show/NCT04295551.
Conexión_Interferon alfa
Vitamina D
Hasta hace poco se consideraba que las únicas funciones de la vitamina D eran las relacionadas con el metabolismo del calcio y fósforo, considerándose necesaria para la prevención del raquitismo en niños, osteomalacia en el adulto y la tetania hipocalcemica. Actualmente se sabe que interviene en otros procesos biológicos, como la respuesta inmune a través de la interacción con el receptor específico que se expresa constitutivamente en células presentadoras de antígenos (CPA) como células dendríticas (CD) y macrófagos, así como en linfocitos T.
Por lo antes mencionado, se considera que la vitamina D puede tener un papel central en la modulación de la respuesta inmune. En la revisión de Martineau (2017) Vitamin D supplementation to prevent acute respiratory tract infections: systematic review and meta-analysis of individual participant data40, se concluyó que la suplementación con vitamina D fue segura y protegió contra la infección aguda del tracto respiratorio en general. Los pacientes que eran muy deficientes en vitamina D y aquellos que no recibían dosis en bolo experimentaron el mayor beneficio. La vitamina D o colecalciferol es una hormona conocida desde 1936.
Se ha propuesto a la Vitamina D como otra manera de contrabalancear el Sistema Renina Angiotensina (SRAA) involucrado en la infección por COVID-19.
La vitamina D reduce la actividad de ECA y aumenta la actividad de ECA2 que tiene efecto protector a nivel pulmonar, restituyendo el balance ECA/ECA2. Restablecer este balance mediante la administración de vitamina D parece clave para reducir eventos respiratorios en modelos experimentales.
Los niveles bajos de vitamina D se asocian a incremento de las infecciones respiratorias y en ensayos clínicos controlados la administración de vitamina D también ha ejercido un efecto protector de infecciones en pacientes sin patología o con enfermedad pulmonar obstructiva crónica.
La idea central de la propuesta de dar Vitamina D a la población general, particularmente a la más expuesta para lograr la elevación de los niveles sanguíneos y tisulares de la Vitamina D, y así generar un balance favorable de algunos componentes del SRAA y también de su propio efecto antiinflamatorio. (1)
(1) Martineau AR Vitamin D supplementation to prevent acute respiratory tract infections: systematic review and meta-analysis of individual participant data https://www.bmj.com/content/356/bmj.i6583
Conexión Vitamina D







